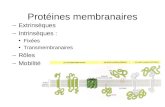
L'eau et le risque biologique - ac-nancy-metz.fr · pourtant une mort par paralysie tétanique des...
Transcript of L'eau et le risque biologique - ac-nancy-metz.fr · pourtant une mort par paralysie tétanique des...
Y-Libes L’eau et le risque biologique
Le risque biologique
1 Notions d’épidémiologie :
1.1 Définitions : Épidémiologie : Science qui étudie les épidémies (« sur la population ») et plus généralement la répartition des maladies humaines. Description des facteurs déterminant la fréquence et la distribution des maladies, leurs origines et les méthodes d'intervention les plus efficaces.
Épidémie : Apparition d'une série de cas comparables dans l'espèce humaine (symptômes et origines), en nombre nettement supérieur à la normale. C'est un phénomène de masse limité dans le temps et l'espace, qui augmente rapidement et disparaît rapidement.Chez les animaux, on l'appelle épizootie. Ces maladies se manifestent sous forme de poussées soudaines et aiguës dans une zone géographique ou un pays.
Pandémie : C'est un phénomène de masse limité dans le temps mais pas dans l'espace. C'est un épidémie qui touche ou moins tout un continent.
Endémie : Ce sont des maladies qui se maintiennent à un taux quasi constant dans une population. Elles sont limitées dans l'espace mais pas dans le temps.
Infection : Pénétration dans un macro-organisme d'un micro-organisme capable de s'y multiplier.
Contagion : Transmission d'une maladie d'un sujet à l'autre par contact direct.
1.2 Notion de chaîne épidémiologique : On parle de réservoir pour décrire le point de persistance et de stockage de la maladie ainsi que son point de départ.Il est fréquemment humain et/ou animal mais peut aussi être hydrique pour les espèces environnementales. Le vecteur est l’éléments utilisé pour la dissémination et /ou la propagation inter/hôte.Il peut être vivant ( ex :moustiques,rongeurs) ou inerte (ex :l’eau).On parle d’Hôte pour l’organisme terminal de la chaîne épidémiologique,celui où la pathologie se développe.Les formes de dissémination peuvent être différentes des formes infectieuses terminales EX : forme de résistance type kyste ou spores. Ex : forme de vie intermédiaire chez les vecteurs dans certains cycles parasitaires. Rem : lors d’une épidémie les individus porteurs de germes (asymptomatiques ou non) deviennent des vecteurs de germes qui pénètrent chez de nouveaux individus.
1.3 Interactions Hôte pathogène : Introduction : La pathologie c’est toute modification de l’état physiologique transitoire ou permanente vers le moins bien qu’elle soit minime ou très importante. On appelle pouvoir pathogène ou pathogénicité d’un micro-organisme une capacité à induire de telles modifications.
Y-Libes L’eau et le risque biologique
Les modalités utilisées par les micro-organismes pour exercer leur pouvoir pathogène sont multiples :
� Si on reprend l’expérience de Griffith : l’injection intra péritonéale de pneumocoques capsulés provoque la mort des souris. Une autopsie montre que le sang est les tissus ont été envahis par les bactéries. Dans ce cas c’est le pouvoir invasif du germe qui provoque le décès. Cette propriét é regroupe toutes les modalités qui permettent la pénétration du micro-organisme dans l’hôte, sa prolifération et sa dissémination.
� Lorsqu’une plaie et souillée par de la terre ou un instrument souillé par des spores de Clostridum
tétanii , les bactéries se développent et restent circonscrites au niveau de la plaie. On observe pourtant une mort par paralysie tétanique des muscles du thorax (action sur les nerfs et les muscles situés à distance).Ces troubles sont reproductibles si on injecte un filtrat de culture de Clostridium tétanii. On peut donc en déduire que c’est la sécrétion de un ou plusieurs composés solubles qui permet cette action à distance du point d’infection. On parle de toxine(s) et de pouvoir toxique (ou toxinogène).
Def : Le pouvoir toxique c’est la capacité à produire une ou plusieurs toxines. Def : La toxine est un composé organique produit par un organisme vivant doté de propriétés antigéniques et capable d’exercer des effets néfastes à distance du point d’infection. Les micro-organismes pathogènes mobilisent de façons diverses ces 2 modalités qui constituent des caractéristiques intrinsèques au germe étudié. La déclaration d’une pathologie dépend également de facteurs extrinsèques. On résumera donc les paramètres influençant la déclaration d’une pathologie sous la forme du triptyque suivant :
Pour tenir compte de cet ensemble de données on sépare usuellement les micro-organismes en 2 classes :
� Les bactéries Pathogènes Spécifiques (BPS) : Elles provoquent une maladie précise chez un hôte dont le système immunitaire est compétent et l’état physiologique normal (Ex : Le bacille du charbon B.Anthracis).On distingue parfois les pathogènes facultatifs qui peuvent exister et se multiplier à l’état libre dans l’environnement et les pathogènes obligatoires qui ne peuvent pas se multiplier hors du foyer infectieux
Etat physiologique de l’hôte. � YOPI’S.
� Traitement médicamenteux. � Prédisposition génétique.
Porte D’entrée.
Micro-organisme : � Pouvoir invasif.
Y-Libes L’eau et le risque biologique
� Les Bactéries Pathogènes Opportunistes (BPO) : Elles sont normalement commensales ou saprophytes et provoquent occasionnellement des pathologies lors de dysfonctionnements physiologiques chez l’hôte ou de leur introduction dans un lieu inhabituel (ex : introduction directe dans le sang par piqûre).Ex : E.coli. ; Klebsiella pneumoniae, Pseudomonas aeruginosa, Acinetobacter….etc.
2 Principaux pathogènes d’origine hydrique : 2.1 Agents bactériens : 2.1.1 Entérobactéries :
� Salmonella : Toutes les salmonelles pathogènes appartiennent à l’espèce salmonella I ou Salmonella enterica. Des variations antigéniques au niveau des sucres de l’antigène O (LPS de la membrane externe) permettant de la subdiviser en différents sérotypes responsables de deux types de Salmonelloses :
Les fièvres typhoïdes et paratyphoïdes (S. typhi, paratyphi et sendai) évoluant spontanément vers la septicémie et où le pronostic vital est en jeu.Elles sont devenues rares dans les pays développés grâce au traitement systématique de l’eau potable.Elle restent présentes dans les pays en voie de développement et réapparaissent dans les pays de l’ex URSS pour des raisons de salubrité évidente.
Les gastro-entérites plus fréquentes et dues à de nombreux sérotypes ubiquistes. Les signes sont beaucoup plus banaux allant des simples troubles intestinaux à la gastroentérite aiguë les évolutions septicémiques sont rarissimes.Les phénomènes de portage sont fréquents. Shigella : Le genre Shigella comporte 4 espèces et plusieurs sérotypes qui sont uniquement pathogènes pour l'homme et les primates.Leur relative résistance au pH acide permet à une faible charge microbienne d’être infectieuse (102 à 103 bactéries environ) On distingue :
S. sonnei, S. flexneri, S. hoydii qui sont responsables de la plupart des cas de gastroentérites aigues dans les pays industrialisés. S. dysenteriae responsables de la dysenterie bacillaire qui est une maladie épidémique grave, de gastro-entérites et de diarrhées d'origine hydrique ou alimentaire
incubation vomissement diarrhée Fièvre Epidémiologie Pathogénie Symptômes cliniques Salmonella sp. (gastro-entérite)
8-48 heures
± ++ + Développement des bactéries dans l'intestin.
Infection superficielle de l'intestin, peu d'invasion. Dose infectieuse supérieure à 105 organismes.
Début graduel ou brutal de diarrhées et fièvre peu élevée, souvent nausée, céphalée et douleurs musculaires. Pas d'antimicrobien sauf si on suspecte une dissémination systémique. Les cultures de selles sont positives pour Salmonella. Portage prolongé fréquent
Y-Libes L’eau et le risque biologique
La bactérie à la propriété de déclencher sa propre phagocytose par les cellules M de l’intestin puis d’échapper au système immunitaire en lysant le phagosome et en colonisant les cellules intestinales de proche en proche.Elle secrète une exotoxine qui inhibe la synthèse protéique dans les cellules du gros intestin et provoque leur destruction d’où des diarrhées mucosanglantes. Shigella dysentriae secrète de plus la toxine shiga qui engendre une fuite d’eau et d’électrolytes au niveau des entérocytes ( composante hydrique plus marquée de la diarrhée), elle peut également évoluer vers des formes septicémiques,alors que les autres espèces restent circonscrites à l’intestin.
� E.coli responsables de gastroentérites : Les bactéries coliformes de laboratoire sont habituellement inoffensives, mais certaines souches peuvent être pathogènes.Toutes les souches pathogènes possèdent des fimbriae spécifiques qui leur permettent d'adhérer à certaines cellules épithéliales de l'intestin. Ces bactéries produisent aussi des toxines responsables de troubles gastro-intestinaux que l'on regroupe sous l'appellation gastroentérite à E. coli. La maladie se contracte par transmission orofécale, soit par ingestion d'eau et d'aliments contaminés, soit par contact avec des objets contaminés. Les individus atteints restent contagieux tant qu'ils excrètent des microorganismes dans leurs fèces. Le manque de propreté et d'hygiène est souvent mis en cause.Il existe plusieurs biotypes d'E. coli pathogènes qui différent par leur virulence et la sévérité des dommages qu'ils provoquent; on distingue ainsi :
� E. coli entérotoxinogène (ECET) � E. coli entéro-invasif (ECEI), � E. coli entérohémorragique (ECVT) � E. coli entéropathogène (ECEP).
Les principaux signes et symptômes comprennent des crampes abdominales et l'apparition de vomissements et de diarrhées entraînant une déshydratation sévère suivie, dans les formes les plus graves, d'un état de choc.Les risques d’origine hydrique concernent essentiellement les ECET et plus rarement les ECEI .
La souche entérotoxinogène n'est pas invasive; la bactérie adhère aux cellules intestinales par
des fimbriæ et sécrète deux types d'entérotoxines responsables d'une diarrhée liquide, abondante, sans présence de sang ni de mucus; leur mécanisme d'action s'apparente à celui de la toxine du choléra.Ce biotype est principalement responsable de la diarrhée des voyageurs (ou tourista)
Salmonella typhi (fièvre typhoïde)
10-14 jours
± ± ++ Les bactéries se multiplient dans l'épithélium de l'intestin et atteignent les ganglions lymphatiques, le foie, la rate, et la vésicule biliaire.
Symptômes dûs aux endotoxines et à l'inflammation, dose infect- tieuse supérieure ou égale à 107 organismes.
.Au début, fièvre, céphalée, malaise, anorexie et douleurs musculaires ; fièvre atteignant 40°C à la fin de la première semaine et durant 2 semaines ou plus ; avec souvent diarrhée, douleurs abdominales, toux et maux de gorge. Maladie raccourcie par l'antibiothérapie.
Y-Libes L’eau et le risque biologique
et, dans les pays en voie de développement, de nombreux cas de diarrhée infantile. L'agent causal n'est pas toujours identifié, mais on soupçonne que de 50 65 % de ces diarrhées sont dues à E. coli entérotoxigène.. La dose infectieuse varie de 108 à 1019 bactéries par ingestion.Les cas de diarrhée des voyageurs attribuables à des souches d'E.coli entéro-invasives sont moins communs. Ces bactéries s'attachent aux cellules épithéliales du côlon et y pénètrent par phagocytose; les bactéries envahissent la muqueuse, l 'enflamment et y provoquent la formation d'ulcères. L'infection entraîne de la fièvre et, parfois, une dysenterie semblable à celle causée par Shigella, soit des diarrhées mucoïdes et parfois sanguinolentes. La bactérie survit facilement dans l'environnement. La dose infectieuse est habituellement de 109 bactéries par ingestion.
� Yersinia enterocolitica : on la rencontre essentiellement dans les pays froids à tempérés (germe psychrophile) et son incidence serait comparable à celle des salmonelles ou des shigelles.C’est un germe entéroinvasif qui provoque des diarrhées purulentes et sanguinolentes assorties de fortes douleurs abdominales.La production d’entérotoxines est rare de même que le passage vers le sang.
2.1.2 Les vibrions :
Les 2 espèces principalement incriminées sont V.cholerae et V.parahémolyticus. Ce sont des germes non invasifs entérotoxinogènes.Leur toxines provoque une fuite massive d’eau et d’électrolyte au niveau intestinal.La guérison est spontanée et le traitement vise à pallier aux effets de la déshydratation.
V.cholerae est halotholérant, si bien qu’il représente un danger tant au niveau des eaux douces que saumâtres.On distingue les sérotypes O1 et O139 qui sont responsable d’épidémies mortelles et les « NON-O1 » responsables de cas isolés et moins graves de diarrhée aqueuse, le plus souvent après ingestion de coquillages ou de crustacés. V.parahémolyticus est halophile et ne se trouve que dans les eaux salées à saumâtres, il est impliqué dans des cas d’intoxication par le poisson cru essentiellement au japon.
2.1.3 Campylobacter : Ce sont les espèces C.coli et C.jejuni qui sont incriminées. Leur incidence à été longtemps sous évaluée à cause des difficultés d’isolement et de culture à partir des selles de malades.On évalue les cas à 2000000 par an aux état unis.Ces germes entéroinvasifs se multiplient au niveau de la muqueuse intestinales et secrète une toxine proche de celle du choléra d’où une inflammation de l’intestin avec émission massive de selles purulentes et sanguinolentes.La guérison est spontanée et le traitement courant vise à pallier à la fuite d’eau et d’électrolytes. 2.1.4 Les mycobactéries « atypiques » : Elles regroupent un très grands nombre d’espèces , autres que M tuberculosis et M leprae, qui se développent dans les eaux stagnantes et les sols humides puis colonisent ensuite tous les écosystèmes aquatiques.Leur très grandes résistance aux traitement physicochimique les rends apte à passer dans le réseau de distribution d’eau et à le coloniser.Elles sont responsables d’atteintes cutanées contractées lors de baignade ou d’atteinte pulmonaires ( mycobactérioses) via les aérosols produits au niveau des robinets, pommeaux de douche…………..etc.Leur incidence est faible. 2.1.5 Legionella : Elle provoque des pneumopathies extensives, graves, accompagnées de signes digestifs (diarrhées, douleurs abdominales), neurologiques,(agitations, hallucinations,...)Les Legionella constituent un vaste groupe de bacilles Gram-, d'environ 5 espèces, dont principale L.pneumophila
Y-Libes L’eau et le risque biologique
est responsable de la majorité des cas. Ces bactéries se trouvent abondamment dans les eaux de rivière, les lacs, les étangs. Leur croissance est favorisée par la température.Elles prolifèrent donc dans les circuits d'eau chaude sanitaire, dans les tours d'aéro-refroidissement, les caissons d'humidification, climatiseurs, avec en plus un effet d'aérosol disséminant.. Ces bactéries ne sont pathogènes que par voie aérienne, leur présence dans les eaux d'alimentation présente donc peu de risques pour la consommation. Par contre, le risque est important au niveau des robinets d'eau chaude et des douches (aérosols) en milieu hospitalier où des malades sont immuno-déprimés. 2.1.6 Aeromonas : Ils peuplent abondamment les eaux usées, les eaux naturelles et les eaux de distribution. Chez l'Homme, ce sont des pathogènes opportunistes qui se manifestent par des gastro-entérites, des diarrhées, des pneumopathies, des septicémies, ... à la suite de baignades en eau douce ou par prolifération dans le réseau de distribution lors des mois chauds d’été. 2.1.7 Leptospirose. : La leptospirose (Leptospira ictero-haemorrhagiae essentiellement) est une infection sévère qui, dans sa forme la plus typique, se présente sous forme d'ictère infectieux à recrudescence fébrile avec signes d'atteinte rénale et méningée. L'évolution comporte une longue convalescence ; parfois l'hépatonéphrite s'aggrave aboutissant à la mort. La transmission se fait par voie transcutanée à la faveur de lésions ou d'excoriations ou même à travers une peau saine hydratée et macérée au contact de l'eau et de la boue ; elle s'effectue également par voie muqueuse soit nasale (bains en rivière) soit conjonctivale (frottement de l'oeil par un doigt souillé), soit enfin digestive (ingestion d'eau contaminée). Le rôle de l'eau est capital et les baignades en rivières ou en étangs représentent une cause fréquente de contamination. La leptospirose est une maladie des vacances, des loisirs, du camping ; elle est aussi une maladie professionnelle pour certains métiers comme les égoutiers, les éleveurs, etc... L'eau d'alimentation est exceptionnellement en cause
2.1.8 Tularémie : La tularémie est une maladie du lièvre et de certains rongeurs (mulots et campagnols chez lesquels elle sévit sous forme de vastes épizooties). La tularémie humaine est liée, à la pénétration de Francisella tularensis à travers la peau ou les muqueuses saines. Suivant la porte d'entrée, les tableaux diffèrents. La forme ulcero-ganglionnaire des membres peut résulter d'un simple contact avec un animal infecté (peau saine) ; la forme oculaire succède à une contamination conjonctivale par les doigts infectés ; la forme angineuse ou amygdalienne est à porte d'entrée digestive ; elle se présente sous forme d'une amygdalite fébrile brutale et douloureuse avec adénopathies (sous-maxillaires et jugulo-carotidiennes). Les eaux de surface (baignades en rivières, étangs), souillées par les rongeurs, peuvent donc transmettre la maladie par contact. L'eau d'alimentation peut être aussi responsable, comme en témoignent les nombreux cas rapportés principalement en Russie et en Europe Centrale, plus rarement aux Etats Unis.
2.2 Agents viraux :
Les virus d’origine hydrique comprennent essentiellement les norovirus, le virus de l’hépatite A (VHA), le virus de l’hépatite E (VHE), les rotavirus et les entérovirus (poliovirus, virus Coxsackie A et B, échovirus et quatre entérovirus non groupés). Les êtres humains sont le seul réservoir naturel de VHA, de norovirus, d’entérovirus et de rotavirus. Le VHE est d’origine zoonotique.Les entérovirus
Y-Libes L’eau et le risque biologique
sont excrétés en grandes quantités dans les matières fécales des sujets humains et animaux infectés (symptomatiques et asymptomatiques), elles peuvent contenir plus d’un milliard (109) de virus par gramme.
Certains, tels les entérovirus sont particulièrement résistants et peuvent survivre au traitement de l’eau potable .Il est en effet possible d’en détecter la présence dans de l’eau potable traitée qui semble ne pas contenir de coliformes. Leur présence dans l’eau potable peut être causée par une désinfection insuffisante ou un traitement inadéquat des eaux de surface contenant de fortes concentrations de virus
Même si les virus ne peuvent se multiplier en dehors des tissus de leur hôte et, par conséquent, dans l’environnement, ils peuvent survivre plusieurs mois dans l’eau douce et pendant des périodes plus courtes dans l’eau salée. Ils survivent plus longtemps dans l’environnement à basse température et en présence de sédiments auxquels ils s’adsorbent facilement. La lumière du soleil, des températures plus élevées et une forte activité microbienne raccourcissent la durée de survie des virus. On a signalé que dans les eaux souterraines protégées où les températures demeurent en général au-dessous de 10 °C, les entérovirus pouvaient survivre presque deux ans. Les eaux souterraines peuvent être contaminées par l’évacuation d’eaux usées domestiques ou de boues sur la terre, par des effluents provenant de champs d’épandage, des eaux de fosses septiques et par l’infiltration d’eaux de surface.
2.2.1 Les Norovirus Le terme norovirus a été approuvé récemment comme nom officiel du groupe de virus
communément appelés virus semblables à Norwalk ou petits virus ronds structurés .Ce groupe de virus inclut une série de quatre petits virus à ARN pathogènes. Ils sont stables dans l’environnement et survivent à la chloration de l’eau, au gel et à des températures allant jusqu’à 60 °C.Les norovirus atteignent les nouveau-nés, les enfants et les adultes. Les effets sur la santé associés aux infections à norovirus ont tendance à être bénins et résolutifs et durent habituellement de 24 à 48 heures. Les nausées, les vomissements, la diarrhée, les douleurs abdominales et la fièvre sont au nombre des symptômes. On ne connaît pas la dose infectieuse, mais on suppose qu’elle est faible. La période d’incubation est de 24 à 48 heures. L’eau, les aliments (et en particulier les mollusques et crustacés et les salades), les aérosols, les vecteurs passifs (objets inanimés contaminés) ainsi que le contact entre personnes .
2.2.2 Virus de l’hépatite
Il y a cinq types de virus de l’hépatite, dont deux seulement (VHA et VHE) semblent se transmettre par la voie fécale-orale et sont associés à la transmission par voie hydrique.
Le VHA est un petit virus à ARN monocaténaire, sans enveloppe et à symétrie icosaédrique. Le VHE est un virion sans enveloppe, et à ARN polyadénylé monocaténaire. Compte tenu de ses caractéristiques physicochimiques, on suppose que le VHA est un calicivirus.L’infection par le VHA est souvent propagée par des aliments ou de l’eau, il constitue la première cause d’hépatite en france. .Les infections à VHA communément appelées hépatites infectieuses, peuvent causer au foie des dommages qui peuvent être mortels. On ne connaît pas la dose infectieuse, mais on la situe dans une plage de 10 à 100 virions. La période d’incubation d’une infection à VHA varie de 10 à 50 jours, elle est inversement proportionnelle à la dose. Les symptômes de la maladie comprennent de la fièvre, des malaises (fatigue), de l’anorexie, des nausées et une gêne abdominale. La jaunisse suit quelques jours plus tard. La maladie est habituellement résolutive, mais le taux de mortalité peut atteindre 2 % chez les adultes de plus de 40 ans. Les sujets infectés excrètent le virus.
Les vecteurs de transmission du VHE comprennent l’eau et le contact entre personnes. La
transmission par voie alimentaire est aussi possible dans leurs matières fécales pendant une à deux semaines avant que l’hépatite se déclare .
Y-Libes L’eau et le risque biologique
La maladie causée par le VHE est appelée hépatite E, ou hépatite non A non B. Sur le plan clinique, on ne peut distinguer l’hépatite E de l’hépatite A. Ses symptômes comprennent des malaises, de l’anorexie, des douleurs abdominales, de l’arthralgie et de la fièvre. La période d’infection de l’hépatite E varie de deux à neuf semaines; l’affection est habituellement bénigne et se résorbe en deux semaines sans laisser de séquelles. Le taux de mortalité s’établit à 0,1-1 %, sauf chez les femmes enceintes où il atteint presque 20 %. La maladie touche le plus souvent des sujets jeunes ou d’âge moyen (15 à 40 ans).
2.2.3 Rotavirus Les rotavirus sont des virus à ARN bicaténaire. Au microscope électronique, les virions intacts
ressemblent à une roue, d’où le préfixe « rota ». On a défini six groupes sérologiques de rotavirus, dont trois (groupes A, B et C) infectent les êtres humains. La gastro-entérite à rotavirus peut se manifester sous des formes variant de la diarrhée bénigne d’une durée de moins de 24 heures à la gastro-entérite grave qui peut être mortelle. Le sujet peut vomir pendant une période allant jusqu’à 48 heures avant l’apparition de la gastroentérite. La période d’incubation varie d’environ 19 heures à deux jours. La maladie dure en général de 5 à 8 jours. On suppose que la dose infectieuse est de 10 à 100 virions
Le rotavirus du groupe A est endémique dans le monde entier et constitue le groupe le plus courant et le plus répandu. Les enfants de six mois à deux ans, les nouveau-nés prématurés, les personnes âgées et les sujets dont le système immunitaire est déficient sont particulièrement vulnérables aux symptômes plus graves causés par l’infection à rotavirus du groupe A. Celui-ci est la principale cause de diarrhée grave chez les nourrissons et les enfants et il cause environ la moitié des cas qui nécessitent une hospitalisation. Dans les régions tempérées, la maladie se manifeste principalement au cours de l’hiver, mais elle est présente pendant toute l’année sous les Tropiques.
2.2.4 Les enterovirus Les entérovirus constituent un grand groupe de virus appartenant au genre Enterovirus et à la
famille des Picornaviridés. Il s’agit de virus à ARN monocaténaire sans enveloppe et à symétrie icosaédrique. Ce groupe comprend les poliovirus (trois sérotypes), les virus Coxsackie A (23 sérotypes) et B (six sérotypes), les échovirus (31 sérotypes) et quatre entérovirus non groupés (types 68 à 71). Ces virus sont très résistants aux agresseurs environnementaux et stables en milieu acide (jusqu’à un pH de 3). La voie orale est la principale voie d’infection par les entérovirus, dont la période d’incubation varie de 2 à 35 jours. Les entérovirus peuvent survivre au transit dans l’estomac et infecter le tractus intestinal inférieur. La virémie est fréquente et le passage dans divers organes cibles entraîne tout un éventail de symptômes. La poliomyélite et la méningite sont les maladies les plus graves causées par les entérovirus, mais on a également incriminé ces derniers dans la myalgie, le syndrome de Guillain-Barré, l’hépatite, les maladies fébriles et la conjonctivite.
2.2.5 Autres virus Les adénovirus sont membres de la famille des Adenoviridés, qui inclut plus de 90 sérotypes,
dont 49 peuvent infecter les êtres humains. Les membres de cette famille comprennent des virus icosaédriques sans enveloppe contenant de l’ADN bicaténaire. Les adénovirus sont très stables dans l’environnement et peuvent survivre longtemps en dehors de l’hôte. Les adénovirus humains peuvent causer des infections respiratoires et gastro-intestinales. La gastro-entérite à adénovirus atteint surtout les jeunes enfants. Sa période d’incubation varie d’un à trois jours et ses symptômes comprennent la diarrhée et les vomissements. Les adénovirus peuvent être transmis par contact direct, par la voie fécale orale ou par les eaux utilisées à des fins récréatives. On n’a pas incriminé l’eau potable comme voie de transmission.
Les astrovirus sont membres de la famille des Astroviridés, qui inclut sept sérotypes capables
d’infecter les êtres humains. Les membres de cette famille comprennent des virus sans enveloppe de 28 à 30 nm contenant de l’ARN monocaténaire. Le microscope électronique révèle leur forme en étoile
Y-Libes L’eau et le risque biologique
caractéristique. L’infection à astrovirus cause habituellement des symptômes qui ressemblent énormément à ceux que l’on observe dans le cas de l’infection à rotavirus et elle atteint surtout les jeunes enfants. Sa période d’incubation varie d’un à quatre jours. Les astrovirus sont transmis par la voie fécale-orale, par les eaux utilisées à des fins récréatives ou par les aliments. On n’a pas incriminé l’eau potable comme voie de transmission.
Les parvovirus sont membres de la famille des parvoviridés, qui inclut deux sérotypes capables
d’infecter les êtres humains. Cette famille inclut des virus icosaédriques sans enveloppe contenant de l’ADN monocaténaire linéaire. Une infection à parvovirus cause habituellement une affection bénine ressemblant à la grippe, parfois accompagnée d’une éruption cutanée. Les complications, qui comprennent l’anémie et l’arthralgi e, peuvent atteindre les femmes enceintes et les sujets dont le système immunitaire est affaibli . La période d’incubation varie de quatre à 14 jours. Des preuves limitées indiquent que le parvovirus est transmis par les aliments (mollusques et crustacés) et les eaux utilisées à des fins récréatives. On n’a pas incriminé l’eau potable comme voie de transmission.
2.3 Protozoaires :
2.3.1 Giardia
La Giardia est un petit parasite protozoaire flagellé que l’on trouve dans l’intestin grêle des animaux et des humains. À l’étape de son développement où elle se nourrit, la Giardia, alors appelée trophozoïte, se trouve principalement dans le duodénum, mais on la trouve fréquemment dans le jéjunum et dans l’iléon de l’intestin grêle. Les trophozoïtes sont généralement attachés à la surface des villosités intestinales par un large disque adhésif ventral (cytostome) .Celui ci leur sert également à se nourrir principalement, pense-t-on, de sécrétions de muqueuses. Lorsqu’il se détache, le trophozoïte binucléé forme un kyste puis se divise au sein de ce kyste, de sorte que quatre noyaux deviennent visibles. Les kystes sont ovoïdes et possèdent deux ou quatre noyaux et présentent des restes d’organelles visibles. Les kystes stables dans l’environnement sont évacués dans les fèces, généralement en grand nombre. Les kystes de Giardia lamblia peuvent survivre jusqu’à 77 jours dans l’eau du robinet à 8 °C mais cette durée diminue à mesure que la température augmente Lorsqu’un hôte favorable ingère ces kystes, le dékystement est provoqué par l’acide et les enzymes de l’estomac; lorsque le parasite atteint le duodénum, une masse quadranucléaire de protoplasme apparaît et se divise rapidement, chaque kyste produisant deux trophozoïtes). L’intestin grêle est alors colonisé par reproduction asexuée.
Giardia lamblia est le parasite intestinal le plus communément signalé dans le monde. On a montré que la giardiase est endémique chez les humains et chez plus de 40 espèces d’animaux, les taux de prévalence allant de 1 à plus de 90 %. Mais l’évaluation reste difficile à cause des cas asymptomatiques.La plupart des foyer d’apparition d’origine hydrique ont été associées à une transmission zoonotique liée aux mammifères, comme le chien, le rat musqué, les bovins et le mouton responsables de l’introduction de kystes dans l’eau de surface utilisée comme source d’eau potable. À mesure que la pression démographique et les activités humaines s’intensifient autour des zones de captage de l’eau, le potentiel de contamination fécale augmente; il faut toujours prendre en considération la possibilité d’une contamination par les eaux usées humaines.Dans ce contexte, il est donc probable que les mammifères jouent pour les humains le rôle de réservoirs de Giardia infectieuse provenant d’une eau contaminée par des eaux usées et qu’à leur tour ils accroissent les concentrations de kystes de Giardia dans l’eau.. La gestion des bassins versants pour contrôler les rejets d’eaux usées et les populations de mammifères aquatiques dans le voisinage des prises d’eau est aussi importante pour prévenir la maladie qu’un traitement adéquat des eaux. Ces épidémies proviennent habituellement d'eaux de surface considérées comme d'excellente qualité, exemptes de contamination fécale, et qui ne font l'objet que d'une simple désinfection au chlore, sans traitement de clarification. Giarda étant enkystée, elle résiste très bien à la chloration et reste contaminante. Un traitement complet avec décantation et filtration lente permet l'élimination
Y-Libes L’eau et le risque biologique
des Giarda.
2.3.2 Cryptosporidium: Le cycle de vie du Cryptosporidium comporte de multiples étapes, typiques des Coccidiés entériques; il se déroule chez un hôte unique et comporte six grandes étapes :
� Le dékystement, au cours duquel les sporozoïtes sont libérés d’un oocyste et adhèrent à la surface épithéliale du tube digestif;
� La mérogonie, au cours de laquelle se produit la reproduction asexuée et la dissémination dans l’hôte;
� La gamétogenèse, au cours de laquelle certains sporozoïtes se transforment en gamète; � La fécondation :Certains de ces gamètes libèrent des microgamètes, qui fécondent d’autres
macrogamètes pour former des zygotes; � La formation des parois de l’oocyste un petit nombre de zygotes conservent une mince paroi
cellulaire, qui se rompt après le développement des sporozoïtes pour entretenir l’infection chez l’hôte. Chez la majorité des zygotes, il se forme une épaisse paroi cellulaire et quatre sporozoïtes, qui deviennent des oocystes et sont évacués dans les fèces.
� La sporogonie, au cours de laquelle se forme le sporozoïte dans l’oocyste.
Étant donné qu’il s’agit d’un agent pathogène transmis par l’eau, l’étape la plus importante de son cycle de vie est celle de l’oocyste rond, à parois épaisses, stable dans l’environnement et d’un diamètre de 4 à 6 µm. On a montré qu’en laboratoire les oocystes du Cryptosporidium survivaient dans les eaux froides (4 °C) pendant une période pouvant atteindre 18 mois et pouvaient résister à toutes sortes de contraintes environnementales, y compris à la congélation (viabilité fortement réduite) et à l’exposition à l’eau de mer.
Le Cryptosporidium parvum est généralement considéré comme étant la principale espèce responsable de la maladie clinique chez les humains et les animaux domestiques; la transmission zoonotique est possible, particulièrement chez les bovins , ovins ,porcs et chevaux qui peuvent eux même être infectés en retour par l’être humain. Les oiseaux aquatiques pourraient également constituer des sources de C. Parvum. Ils seraient contaminés par les oocystes infectieux présents dans leur habitat et ils les transporteraient et les déposeraient dans l’environnement, y compris dans les approvisionnements d’eau potable.
Le symptôme généralement associé à la maladie est la diarrhée, caractérisée par des selles très aqueuses et non sanglantes. Le volume de diarrhée peut être extrêmement important, 3 L/jour étant commun; on a rapporté des valeurs atteignant 17 L/jour . Ce symptôme peut s’accompagner de nausées, de vomissements (particulièrement chez les enfants), de température subfébrile (inférieure à 39 °C), d’anorexie et de déshydratation., de céphalées et des douleurs musculaires
La durée de l’infection dépend de l’état du système immunitaire; on peut la répartir en trois
catégories: (1) celle des personnes immunocompétentes qui se débarrassent de l’infection en 7 à 14 jours, (2) celle des personnes atteintes du SIDA ou dont le système immunitaire est fortement affaibli qui, dans la plupart des cas signalés, ne se débarrassent jamais complètement de l’infection (qui peut se transformer en infection caractérisée par de longues périodes de rémission suivies de symptômes légers) et (3) celle des personnes immunodéprimées à la suite d’une chimiothérapie, d’une dépression ou d’une maladie de courte durée ou d’une malnutrition., l’infection disparaît généralement (aucune excrétion de kystes et les symptômes disparaissent) dans les 10 à 15 jours qui suivent le retour à la normale du système immunitaire, bien qu’on ait signalé des cas d’enfants chez lesquels l’infection a pu persister pendant 30 jours. La sensibilité du diagnostic de la cryptosporidiose par examen des selles est faible, de sorte que les individus qui excrètent peu d’oocystes peuvent être prématurément classés parmi les cas négatifs. Les individus immunocompétents sont généralement porteurs de l’infection pendant une durée maximale de 30 jours et peuvent continuer à transmettre les oocystes pendant une durée pouvant atteindre 24 jours
Y-Libes L’eau et le risque biologique
2.3.3 Les amibes Les Acanthamoeba sont des amibes en liberté que l’on trouve dans toutes sortes d’environnements, y compris le sol, l’air et l’eau. On en a détecté la présence dans des environnements aquatiques, y compris des piscines et de l’eau potable chlorées .Les souches purement environnementales présentent un danger indirect du fait qu’elles peuvent héberger des agents pathogènes opportunistes (p. ex., Legionella pneumophila, Mycrobacterium avium. Ainsi, si des kystes d’Acanthamoeba survivent au traitement de l’eau et pénètrent dans l’eau potable, ces bactéries pathogènes symbiontes pourraient être la cause de maladies chez des êtres humains.De façon plus anecdotique Naegleria fowleri est une amibe responsable de méningo-encéphalites. Elle colonise les condenseurs en inox des centrales nucléaires. Il ne faut dont pas se baigner en aval des rejets.Sous les latitudes sub et intertropicales (Asie, Afrique) , Entamoeba histolytica est responsable de la dysenterie amibienne. La contamination se fait par ingestion alimentaire ou par les kystes par voie hydrique. Les kystes peuvent donner naissance à une amibe pathologique hématophage et nécrosante qui provoque des altérations de la paroi intestinale. Les diarrhées afécales avec des glaires et du sang sont fréquentes. Si l'amibe pénètre dans l'organisme, elle provoque des abcès du foie, des poumons, du cerveau...
Ce sont leurs kystes qui posent problème dans la mesure où ils résistent aux concentrations habituelles de chlore.
Y-Libes L’eau et le risque biologique
Le cycle de Giardia lamblia
multiplicationpar seission binairedans l'intestin grêle
désenkystementdans la partie proximale
de l'intestin grêle
trophozoïtesdans la muqueuse de l'intestin grêle
kyste
kyste
kyste
trophozoïte
formes excrétées
destruction
INGESTION
EXCRETION
HOTE
MILIEUEXTERIEUR
Y-Libes L’eau et le risque biologique
Le cycle d’ Entamoeba histolytica
1 2
1-Cycle non pathogène d’Entamoeba histolytica. Il aboutit à la dissémination des kystes dans la
nature.
2- Cycle pathogène d’E.histolytica. L’Amibe est hématophage mais ne s’enkyste pas.
3- Mécanisme de la formation de la lésion amibienne élémentaire au niveau du colon
A- L »’amibe pénètre au niveau dans la muqueuse à la faveur d’une lésion préexistante (bactérienne ou mécanique).
B- Elle s’y multiplie et lyse les cellules.
C- Elle détermine dans la sous-muqueuse la formation d’un abcès
D- qui se vide dans la lumière intestinale par un pertuis : c’est l’abcès en bouton de chemise.
E- Elle peut également passer dans les capillaires mésentériques. C’est la point de départ des localisations de métastases.
Y-Libes L’eau et le risque biologique
2.4 Les helminthes : Ce sont les vers parasites intestinaux et/ou tissulaires de l’homme et des animaux, selon leur mode de transmission à l’homme on distingue trois groupes :
� Groupe 1 : Ils sont transmis par ingestion d'un hôte intermédiaire : � Groupe 2 : Les larves infectantes sont capables de traverser la peau ou les muqueuses d'où
des problèmes avec les eaux de lavage et de baignade � Groupe 3 : Transmission par des oeufs ou des kystes infectants. Il faut donc éviter les
contaminations fécales ou filtrer l'eau. Vu. leur taille ils sont éliminé lors des étapes de filtration de l’eau.En revanche en cas de défaillance à cette étape, ils sont insensibles aux doses habituellement utilisées pour la désinfection de l’eau.Ils posent problème essentiellement au niveau des eaux non traitées quels que soit leurs utilisation. Les organismes pouvant participer au risque hydrique sont essentiellement :
� Pour les nématodes ( vers ronds ): Ascaris(GP3) , oxyures, filaires(GP1), ankylostomes, anguillules.
� Pour les cestodes ( vers plat, aspect rubané) : Ténia (taenia), Bothriocéphale(GP1). � Pour les trématodes ( vers plats, non annelés, aspect foliacée) : Bilharziose(GP2) et
Douve du foie(GP3 ou GP1).
Y-Libes L’eau et le risque biologique
Comparaison Entre deux agents « typiques » des groupes 2 et 1 : Les
douves et les schistosomes.
DOUVES SCHISTOSOMOSE Voie d’infestation Buccale avec les aliments Transcutanée contacts avec l’eau
douce Fréquence de l’infestation Dépend uniquement des
habitudes alimentaires locales Dépend uniquement des possibilités de contact avec l’eau (agriculture irriguée, bains, lavage du linge)
Pathogénicité Au contact des épithéliums Au contact des endothéliums Réactions des tissus parasités Pseudo-adénome Pas de modification de
l’endothélium Caractères des adultes hermaphrodites Sexes séparés Caractères des oeufs Toujours operculés
Dépourvus d’éperon Jamais operculés Toujours pourvus d’éperon
Succession des formes larvaires Œuf souvent non embryonné dans les excrétats humains
↓ Miracidium (dans l’eau)
↓ Sporocyste (chez le mollusque)
↓ Rédie (chez le mollusque)
↓ Rédie-fille (chez le mollusque)
↓ Cercaire à queue simple dans
l’eau ↓
Métacercaire intestante enkystée
Œuf toujours embryonné dans les excrétats humains
↓ Miracidium (dans l’eau)
↓ Sporocyste (chez le mollusque)
↓ Sporocyte-fille (chez le
mollusque) ↓
Cercaire à queue bifide (furcocercaire) dans l’eau. C’est la forme intestante.
Y-Libes L’eau et le risque biologique
Cycle d’un parasite « typique » du groupe 2
CARACTERES ESSENTIELS DES SCHISTOSOMOSES HUMAINES Nom du parasite S.haematobium S.mansoni S.japonicum S.intercalatum Répartition géographique
Toute l’Afrique, Madagascar,
Proche et moyen Orient
Afrique Centrale, Antille,
Amérique du Sud
Japon, Chine,
Formose, Philippines,
Célèbes
Afrique centrale
invasion discrète Fièvre + douleurs Toxémie Discrète Lieu de ponte des femelles
Veinules des plexus péri-
vésicaux
Surtout les veinules des plexus mésentériques, en particulier du colon pour S.m. et S.j. rectum pour S.i. mais aussi
artérioles pulmonaires pour s.J. Complication Cystite et
hématurie urétro-pyélo-néphrite Cancérisation
Polypose recto colique,
hémorragies et syndrome de banti
Atteinte viscérale diffuse, cirrhose, anémie, troubles
nerveux, cachexie
Douleurs diarrhée
mollusques bullin planorse onchomélanie Physopsis Animaux « réservoirs de virus »
homme Homme et accessoirement les singes et rongeurs
Homme, bétails, pors, carnivores et
rongeurs domestiques et
sauvages
homme
Y-Libes L’eau et le risque biologique
Cycle d’un parasite « typique » du groupe 1
Cycle évolutif de la Grande Douve (Fasciola hepatica). 1- Les œufs sont disséminés dans la nature par des déjections du bétail. 2- Ils doivent séjourner dans l’eau pour s’embryonner. Lorsqu’ils sont mûrs. 3- Ils éclosent en libérant une larve nageuse ciliée :le miracidium. 4- Celui-ci pénètre chez l’hôte intermédiaire, le mollusque d’eau douce Lymna
truncatula. 4’ Dans la cavité respiratoire, il se transforme en sporocyste dans lequel bourgeonnent des (4’’) rédies qui gagnent l’hépatopancréas ; en été les rédies auparavant, une génération de rédies – filles. 4’’’ Dans le corps des rédies établies dans l’hépatopancréas bourgeonnent des cercaires.
5- Qui quittent le mollusque par effraction et nagent dans l’eau jusqu’à ce qu’elles se fixent sur un support.
6- A ce niveau, elles s’enkystentsous forme de métacercaires qui sont la forme infestante.
7- L’homme s’infeste en consommantcru du cresson sauvage. 8- La jeune douve est libérée de sa coque dans l’estomac. 9- Elle gagne le foie en rampant dans le péritoine et s’établit dans le canal
biliaire. 10- Les œufs sont éliminés par la bile puis dans les selles.
Y-Libes L’eau et le risque biologique
Caractères essentiels des principales distomatoses humaines
Nom du parasite Grande Douve Douve de Chine Douve des félins Douve des poumons Douve de l’intestin Répartition géographique
Europe, importé en Afrique, Amérique et Australie
Extrème Orient, Chine, Japon, Tonkin
Europe centrale et orientale
Extrême Orient Afrique centrale
Extrème Orient
Localisation Canaux biliaires intra hépatiques Poumon Intestin Principaux signes cliniques
Douleurs et fièvre lors d’invasion d angiocholite par poussée
Invasion discrète puis angiocholite ictère
Angiocholécystite Invasion discrète
Dyspnée, toux, crachats « rouillés »
Diarrhée fétide, anémie douleurs
complications Ictère par rétention Cirrhose, cancer du foie Peu de complications pancréatites
Hémoptysie Sclérose pulmonaire IVD
Œdème cachexie
mollusque Lymnea truncatula Diverses dithynia mélania Divers planorbes Aliments contaminateurs
Cresson sauvage Poissons d’eau douce, surtout Cyprins ( tanche, ide, poisson rouge, gardon)
Ecrevisse et crabe d’eau douce
Châtaigne d’eau, racines aquatiques
Animaux »réservoirs de virus »
Bétails surtout ovins et bovins
Tous les félins domestiques et sauvages, chiens porcs et petits carnivores sauvages, rongeurs surtout rats
Porcs, tous les carnivores
Porcs
Y-Libes L’eau et le risque biologique
Cycle d’un parasite « typique » du groupe 3 Cycle évolutif de l’ASCARIS (Ascaris lumbricoïdes).
1- Les adultes vivent dans le grèle 2- Les femelles pondent des œufs qui sont disséminés dans la nature avec les
selles. 3- Ils s’embryonnent durant leur séjour dans le milieu extérieur. 4- Les œufs contenant la larve infestante souillent les légumes et les fruits
poussant à terre. 5- Ils sont avalés avec ces aliments. 6- Les œufs éclosent dans l’intestin grêle et les larves traversent la paroi entérale. 7- Elles gagnent le foie par le système porte ou en cheminant le long des mésos. 8- Elles passent dans le poumon puis remontent jusqu’au carrefour aérodigestif
où elles sont dégluties et deviennent adultes dans le grêle. Principaux accidents et incidents digestifs de l’ascaridiase.
1- Ascaris s’engageant dans l’aampoule de Vater. 2- Engagement du ver dans le cholédoque. 3- Engagement du ver dans le canal hépatique ou dans l’une de ses branches. 4- Migration dans la vésicule. 5- Migration dans le canal de Wirsung. 6- Remonter de l’ascaris dans le duodénum ; il peut forcer le pylore et être vomi. 7- Perforation sans péritonite avec migration à distance dans la grande cavité
péritonéale ou en arrière. 8- Perforation avec péritonite aigue. 9- Perforation avec péritonite plastique, enkystée ou « abcès vermineux ». 10- Occlusion intestinale aigue 5OIA° par obstruction. 11- OIA par volvulus sur un paquet d’ascaris ou un ver seul. 12- OIA par invagination. 13- OIA par étranglement herniaire. 14- Engagement ascaridien dans l’appendice. 15- Migration de l’ascaris dans le colon d’où il sera expulsé par les selles. 16- Abcès ascaridien du foie.