La Tuberculose Pulmonaire Fxl 12 02 08
-
Upload
raymondteyrouz -
Category
Documents
-
view
4.118 -
download
0
Transcript of La Tuberculose Pulmonaire Fxl 12 02 08

Actualités sur la Tuberculose
Docteur F.X LEBASChef de Service du Centre Hospitalier du Mans
FMC du Mardi 12 février 2008


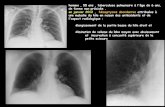
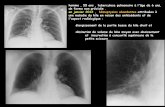
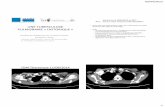
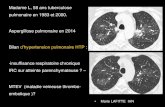
Transmission et contagiosité Tuberculose pulmonaire
• Mycobacterium tuberculosis (rarement africanum et bovis) • Réservoir exclusivement humain• Transmission par voie aérienne (toux, parole, éternuement)• Particules de 1-5 microns (qui restent en suspension)• Contagiosité principalement des malades à BK+ au direct• Rôles de la promiscuité et de la durée d’exposition
30% des sujets « hautement exposés » développeront une tuberculose primaire (PIT)
Un malade (BK+ au direct) infecte 10 personnes /an pendant 3 ans



Histoire naturelle (I)
Foyer parenchymateux limité ± adénopathie satelliteDissémination hématogène possible (foyers secondaires)
Réaction épithélioïde et lymphocytaire, parfois nécrose caséeuse, puis calcification
Généralement asymptomatique et « guérison » spontanée en 6 mois avec persistance de BK « quiescents ».
Développement d’une réponse immune à médiation cellulaire en 2- 10 semaines (virage RCT)
Tuberculose primaire : Infection Tuberculeuse Latente ( ITL)

Histoire naturelle (II)
Evolution de l’ ITL vers une tuberculose maladie :10 % (40% chez les moins de 5 ans) dont 5% dans les 2 premières années.
Réactivation de lésions tuberculeuses quiescentes au-delà des 2 premières années chez 5 % des ITL.
Réinfection exogène : chez les sujets ( les plus) âgés.
Au total, 10% des PIT non traitées chez l’adulte développeront une tuberculose maladie (pulmonaire ou extra-thoracique) .
Tuberculose maladie

Histoire naturelle (III)
• Origine ethnique : pays à forte endémie: Afrique SS, Asie du SE, Indes…• Age: moins de 5 ans et augmentation après 30 ans.• Malnutrition, conditions socio-économiques défavorables: PRECARITE….• Diabète• Silicose• Immunodépression (++) : CS, IRC, hémopathies, HIV++, greffes d’organes.
Tuberculose maladie: facteurs de risque

Epidémiologie (I)
Estimations mondiales..le fléau
Population infectée: 2000 millions (1/3)Incidence estimée: 8 millions / an Mortalité: 2 millions / an (6.7% des décès)
5ème cause de mortalité..25% des décès « évitables » dans les pays en développement

Epidémiologie (II)
Variations géographiques de l’incidence(taux pour 100,000 habitants)
Pays industrialisés 5-50Afrique 220Sud est asiatique 200Pacifique et Chine 200Méditerranée orientale 155Amérique latine 120
France: 10 (mais IDF: 30)
1994: 16.8 – 1996: 13.1 – 1998: 11.4

Incidence de la Tuberculose dans le Monde

How much TB in Cambodia? Estimates for 2001
estimateestimate number number rate/100,000 rate/100,000incidence (all)incidence (all) 75,00075,000 573 573incidence HIV 9,200incidence HIV 9,200 70 70incidence (ss+) 34,000incidence (ss+) 34,000 256 256prevalence (all) 178,000 prevalence (all) 178,000 1356 1356prevalence (ss+) 72,000prevalence (ss+) 72,000 548 548 deathsdeaths 16,000 16,000 121 121

Epidémiologie (III)
Les causes de la reprise transitoire de 1990 dans les pays industrialisés et de la pandémie mondiale..
• Accroissement démographique• Migrations à partir de pays à endémie élevée• Pandémie de VIH (coinfection ++)• Pauvreté et inégalité d’accès aux soins• Baisse des ressources allouées aux programmes de contrôle • Oubli des principes de traitement (pays industrialisés)

14
La tuberculose dans le monde
Estimated TB incidence rates, 2004
The boundaries and names shown and the designations used on this map do not imply the expression of any opinion whatsoever on the part of the World HealthOrganization concerning the legal status of any country, territory, city or area or of its authorities, or concerning the delimitation of its frontiers or boundaries.Dotted lines on maps represent approximate border lines for which there may not yet be full agreement. WHO 2005. All r ights reserved
0 - 2425 - 4950 - 99100 - 299
Noestimate
300 ormore
Estimated new TBcases (all forms) per100 000 population

TUBERCULOSEincidence et mortalité (p 100 000)
1900
1910
1920
1930
1940
1950
1960
1970
1980
1990
2000
1
10
100
1000
mortalité Franceincidence France DGSincidence France SSincidence France consultationsmortalité Mondeincidence Monde

Bull Epid Hebd 2004, 4 :13-16Bull Epid Hebd 2004, 4 :13-16

17
Cas déclarés de tuberculose maladie par Région, 2005 (Nombre de cas et taux)
20
9 8 8 8 7 7 7 7 7 7 6 6 6 6 6 6 6 5 5 5 5 5 4 4
44
0
250
500
750
1000
1250
1500
1750
2000
2250
2500
No
mb
re d
e c
as
0
5
10
15
20
25
30
35
40
45
50
Ta
ux
po
ur
10
0 0
00
Nombre de cas
Taux pour 100 000
Source: InVS, déclaration obligatoire de tuberculose

Morbidité et mortalité* liées à la tuberculose, France métropolitaine,
1972-2005
9,2/105
22,4/105
Sources: InVS (déclaration obligatoire), INSERM (CépiDc)
60,3
* Tuberculose en cause principale de décès
0
10
20
30
40
50
60
70
Années
No
uve
aux
cas
po
ur
100
000
Maladie
Décès30,5
8,9
3,7
1,6

19
Incidence (taux pour 100 000) de tuberculose par département, France entière, 2004
Source: InVS, déclaration obligatoire de tuberculose



Incidence en Pays de Loire


Un programme en six axes
1. Assurer un diagnostic précoce et un traitement adapté pour tous les cas de TM
2. Améliorer le dépistage de la TM et les enquêtes autour d'un cas
3. Optimiser l'approche vaccinale
4. Maintenir la résistance à un faible niveau
5. Améliorer la surveillance épidémiologique et les connaissances sur les déterminants de la TB
6. Améliorer le pilotage de la lutte antituberculeuse

IDR
Reflète l’existence d’une hypersensibilité retardée résultant de l’infection tuberculeuse (et du BCG)
Injection intradermique stricte (++) de 10 unités (0.1 ml) de tuberculine purifiée (avant-bras): papule d’aspect « en peau d’orange » de 6-10 mm
Lecture à 48-72 h: diamètre transversal de l’induration
Autres techniques (timbre, bague..): peu sensibles
Signification, technique, réalisation

IDR
Sensibilité imparfaite (causes techniques, affections associées, effet « temps »)
Spécificité bonne mais non absolue: autres mycobactérioses, effet « rappel »
N’est un indicateur que de l’infection tuberculeuse
Interprétation difficile après BCG
Limitations

IDR
La réalisation d’une IDR n’a d’intérêt que si le résultat détermine l’attitude thérapeutique (traitement d’une infection tuberculeuse latente, suspicion de tuberculose maladie à BK-) ou justifie une surveillance particulière (cas contacts) .. ou entre dans le cadre des dispositions légales (article R215-4 du CSP après vaccination par le BCG)
Une évidence..

IDR
Reste difficile..et variable d’un pays à l’autre (!)
Doit prendre en compte:- Résultats de tests antérieurs (lorsqu’ils existent..)- Statut vaccinal (qui complique l’interprétation en France)- Affections associées (notamment VIH)
Interprétation

IDR
Reste difficile..et variable d’un pays à l’autre (!)
Doit prendre en compte:- Résultats de tests antérieurs (lorsqu’ils existent..)- Statut vaccinal (qui complique l’interprétation en France)- Affections associées (notamment VIH)
Interprétation

IDR en Résumé
Manque de sensibilité : faussement négatif (10 à 25 %)
• immunodépression sous jacente :
cancer, dénutrition, immuno-dépression, infection virale ou vaccination par virus vivant, insuffisance rénale, sarcoïdose, vieillissement, VIH …
• tuberculose très active altérant capacités immunologiques
miliaire
Manque de spécificité : faussement positif (35 à 60 %)
• vaccination antérieure par BCG
• exposition à mycobactéries environnementales

DISTRIBUTION COMPOSITE RESULTANT DE RÉACTIONS SPÉCIFIQUES ET NON-SPÉCIFIQUES À LA TUBERCULINE
Induration (mm)
0 5 10 15 20 25 30 35
No
mb
re d
e ré
acti
on
s
0
20
40
60
80
100
Rieder HL. Tuber Lung Dis 1995;76:114-21
Seuil du test
pas d'infection mycobactérienne
infection par mycobactérie tuberculeuse
infection par mycobactérie non-tuberculeuse

IDR
RCT 10 mm (sans notion sur l’ancienneté de l’infection)OU
RCT 5mm (si notion d’une IDR antérieure négative)OU
IDR1 (<2ans) <10mm et IDR2>10mm et différence 10mm
Critères de positivité - Sujet non vacciné

IDR
Différence RCT ancienne (<2ans) - RCT actuelle 10mmOU
RCT 10mm si BCG > 10 ans (VPP: 88%)OU
Positivation (critère 1) sur un contrôle effectué à 2 mois (mais attention à l’effet « booster » après 55 ans)
Noter que l’IDR est peu contributive au diagnostic d’infection tuberculeuse par BK « sauvage » dans les 10 ans qui suivent la vaccination..
Critères de positivité - Sujet vacciné


TESTS INTERFERONTESTS INTERFERON
Cellestis (Australie) • QuantiFERON® TB Gold
• Approuvé par la FDA en décembre 2004
Oxford Immunotec (Royaume Uni)• T-SPOT.TB®

TESTS INTERFERONTESTS INTERFERONRationnel Immunologique
• Ag (ESAT-6 et CFP-10) spécifiques de M. tuberculosis, M. kansasii, M. marinum, M.
szulgaï non présent sur les autres Mycobactéries, dont le BCG
• production d’interféron γ après stimulation des lymphocytes T des sujets infectés stimulés par ces Ag
QuantiFERON® Technology

CFP-10 and ESAT-6 IFN- assay and Mantoux tuberculin test, stratified by age, for 110 patients with culture-positive TB
Age (yr)
No.
IFN-γ tested
No.
IFN-γ positive
Percent
IFN γ -positive
No.
Mantoux-tested
No.
Mantoux-positive
Percent
Mantoux-positive
13–30 19 17 89.5 9 9 100.0
31–40 14 14 100.0 12 7 58.3
41–50 16 15 93.8 12 9 75.0
51–60 19 19 100.0 10 5 50.0
61–70 19 17 89.5 12 9 75.0
71–80 13 12 92.3 11 6 54.5
> 80 10 8 80.0 6 1 16.7 AJRCCM 2004 170. pp. 59-64

Indication du dosage de l’ interferon gamma: HAS
1: Enquête autour d’ un cas chez l’ adulte 2:aide au Dg des formes extra pulmonaires 3: avant Traitement anti TNF Alpha 4: Embauche des professionnels de Santé

Diagnostic DE LA TUBERCULOSE

PIT symptomatique
Anomalies radiographiques isolées le plus souvent (lésion parenchymateuse du LI ou du segment antérieur du LS, adénopathie hilaire, atélectasie (ADN compressive) Parfois signes cliniques: asthénie, fébricule, érythème noueux, kérato-conjonctivite
Rare..

Infection TuberculeuseTableau Radio-Clinique
Le plus souvent asymptomatique Sinon signes cliniques et/ou radiologiques
syndrome infectieux, voire splénomégalie asthénie, anorexie, amaigrissement érythème noueux kératoconjonctivite phlycténulaire adénopathies cervicales, submaxillaires... chancre d'inoculation, adénopathies atélectasie pleurésie

Tuberculose maladie
Réactivation ± tardive d’un foyer cicatriciel quiescent résultant d’une PIT ; plus rarement: évolution immédiate d’une PIT ou réinfection exogène
Tuberculose pulmonaire : 85%
Tuberculoses extra-respiratoires : 13-15% (ganglionnaire, pleurale et uro-génitale surtout, ostéo-articulaire et neuro-méningée plus rarement)
Tuberculoses multiviscérales : 1-2%

Tuberculose pulmonaire
Asymptomatique (20%): découverte radiographiqueDans 80% des cas symptômes généraux (fièvre, amaigrissement, sueurs) et/ou respiratoires (toux, expectoration, hémoptysie) absolument aspécifiques
Lésions radiologiques souvent assez évocatrices par:- leur siège: LS (apical et dorsal) et segment apical du LI- leur aspect: nodules, infiltrats hétérogènes parfois excavésPlus rarement: pleurésie, miliaire, «pneumonie», aspects séquellaires (parfois difficile)
Symptomatologie



















Tuberculose pulmonaire
Diagnostic bactériologique
Prélèvements - Expectoration ou tubage (x 3) en 1ère intention- Fibroscopie (2ème intention)
Étapes- Examen direct (contagiosité): BAAR en coloration de Zielh Nielsen- Culture : Loewenstein (4 semaines), Bactec (2 sem)-Antibiogramme (4-6 semaines après culture)

Tuberculose pulmonaire
Autres techniques diagnostiques
Amplification génomique par PCRTrès rapide pour de très faible quantité d’ADNInterêt en cas de forte suspicion clinique avec BAAR –Mais Faux Positifs +++ si mycobactérie atypique
Anatomo-pathologie (bronchique, pleurale, ADN) Granulome épithélio-gigantocellulaire, nécrose caséeuse

Populations bacillaires
Bacilles extracellulaires (film liquidien de surface des cavités)- population prédominante, multiplication active- responsables de la symptomatologie et de la contagiosité- médicaments actifs: INH, RMP, SMY
Bacilles intracellulaires (macrophages)- médicaments actifs: PZA, RMP (et à un moindre degré INH)
Bacilles extracellulaires au sein du caséum- seul médicament actif: PZANB: Les bacilles sans activité métabolique sont pratiquement inaccessibles aux antituberculeuxet peuvent persister sous forme quiescente très longtemps et se réactiver

Antituberculeux majeurs
Isoniazide (INH)
Posologie (adulte): 5 mg/kg/j (adaptation en fonction du taux circulant selon la vitesse d’acétylation discutée si insuffisance hépatique, éthylisme, sujet âgé)
Surtout actif sur les BK extracellulaires de surface (stérilisation rapide)
Peu coûteux et dans l’ensemble bien toléré- toxicité hépatique (transaminases, hépatite vraie rare)- polynévrite sensitivo-motrice, troubles neuro-psychiques- syndrome épaule-main, syndrome rhumatoïde
Résistance primaire variable selon les pays (++): 2-25%

Antituberculeux majeurs
Rifampicine (RMP)
Posologie (adulte): 10 mg/kg/j (max 600 mg)
Actif sur les BK extracellulaires et intramacrophagiques
Inducteur enzymatique ++: interactions médicamenteuses(OP, AVK, hypoglycémiants oraux, méthadone, etc..)
Effets secondaires rares, médicament coûteux..- Troubles digestifs- Réactions immuno-allergiques (prises discontinues surtout)- Colore les excrétas (larmes, urine, sueur, sperme) ++

Antituberculeux majeurs
Pyrazinamide (PZA)
Posologie (adulte): 25 mg/kg/j
Actif sur les BK intramacrophagiques et du caséum (prévention des rechutes et raccourcissement de la durée du traitement ++)
Effets secondaires- Toxicité hépatique (< à celle de l’INH)- Hyperuricémie le plus souvent asymptomatique- Photosensibilisation
CI, relatives et variables selon les pays: grossesse (en France..), insuffisance rénale, insuffisance hépatique

Antituberculeux majeurs
Ethambutol (EMB)
Posologie (adulte): 20-25 mg/kg/j
Bactériostatique seulement sur les BK extracellulaires et intramacrophagiques
Effets secondairesNévrite optique rétrobulbaire (dyschromatopsie puis baisse de l’acuité visuelle) : traitement prolongé et à dose élevée surtout, intoxication éthylique, insuffisance rénale

Principes généraux du traitement
Association d’au moins 3 médicaments (afin d’éviter la sélection de mutants plus que pour synergie..)
Une prise unique le matin à jeun (mais seule l’absorption de la RMP est meilleure à jeun..)
Traitement prolongé au moins 6 mois (parfois plus, cf les schémas actuellement préconisés)
Check: CI, interactions médicamenteuse, effets secondaires, observance (uricémie, couleur urines, dosages éventuels)
Éviction: 15 jours après début du Tt (si BK+ au direct)

Régimes thérapeutiques
6HRZ: INH+RMP+PZA 2 mois, INH+RMP 4 mois (+++)
6HREZ: adjonction d’EMB les 2 premiers mois (ou jusqu’à ABGR si possibilité de résistance à l’INH++): traitement antérieur, taux de résistance primaire >4-5%
9HRE: INH+RMP+EMB 3 mois, INH+RMP 6moisCI à l’utilisation du PZA (9 mois de Tt alors nécessaire)
Taux de rechute : 1-2% à 2 ans, <5% à long termeFréquence des effets secondaires: 3-4%Négativation des cultures: 35% à 1 m, 85% à 2 m, >95% à 3 m
Intérêt des spécialités associant plusieurs médicaments

Bilan pré thérapeutique
Bilan biologique hépatique, créatinémie, uricémie (si PZA)NFS avec plaquettesBilan ophtalmologique (si EMB)

Surveillance
Clinique: symptômes respiratoires et généraux, effets secondaires, observance (1 mois, 3 mois, 6 mois)
Radiographie thoracique: 3 mois et fin de traitement (souvent en plus à 1 mois en France..)
Bilan hépatique hebdomadaire pendant le 1er mois (discuté au delà sauf FDR..) : accepter transaminases < 5N (35%), arrêt INH et PZA si > 5N, et de tous les médicaments si hépatite symptomatique
Bactériologie mensuelle jusqu’à négativation (85% à 2m)

Cas particuliers
Grossesse: 9HRE (en France et aux US..) mais PZA accepté par l’OMS et en Grande Bretagne
Insuffisant rénal: PZA CI si IR sévère, adaptation des doses d’EMB et de PZA dans les autres cas (et INH si ClCr < 10 ml/min), vitamine B6
Insuffisant hépatique: CI au PZA si sévère, surveillance accrue, adaptation dose INH (non consensuel), vit B6
Rechutes: au cas par cas selon la qualité du traitement initial, les médicaments initialement utilisés, la notion ou non de résistance..

Prévention
Diagnostic et traitement précoce des formes contagieuses
Déclaration obligatoire (rapide++) ; dépistage et chimioprophylaxie éventuelle des cas contact après enquête et évaluation (environnement, FDR des cas contact..) par MT ou services médico-sociaux spécialisés
Dépistage dans groupes à risque
Vaccination par le BCG..en rediscussion (abandonnée partiellement voire complètement dans certains pays)
Prévention des tuberculoses nosocomiales

Infection Tuberculeuse LatenteIndications de la chimiothérapie chez l’Immunocompétent
enfant si IDR > 15 mm ou phlycténulaire si vacciné par BCG et si (IDR comprise entre 10 et 15 mm et
très fort risque d’infection) si non vacciné par BCG et si (IDR > 10 mm ou phlycténulaire)
ou si (IDR > 5 mm et très fort risque d’infection)
adulte
si IDR > 15 mm et sujet âgé < 80 ans si IDR > 10 mm et si (très fort risque d’infection ou infection
récente) si migrants en France de moins de 2 ans, originaire d’un pays
à forte endémie tuberculeuse

LA CHIMIOPROPHYLAXIELA CHIMIOPROPHYLAXIE
• chez l’enfant
de moins de 2 ans :
INH 10 mg/kg/j et RMP 10 mg/kg/j pendant 3 mois,
de plus de 2 ans :
INH 5 mg/kg/j et RMP 10 mg/kg/j pendant 3 mois,
• chez l’adulte
INH 5 mg/kg/j pendant 9-12mois
ou INH 5 mg/kg/j et RMP 10 mg/kg/j pendant 3-4 mois,
• chez l’immunodéprimé
INH pendant 9 mois.


CONSEQUENCE DE L’ARRET DU MONOVAX
BCG intradermique plus efficace :95 % versus 75 % de virage de l’IDR
Seringues (reprendre 0,05 ml ou 0,1 ml selon l’âge) :mal adaptéesUtiliser des aiguilles courtes ( 1 cm ) biseautées
ultrafines( calibre 26 G / 0,45 mm )
Médecins : ont perdu l’habitude des IDR
Tolérance acceptable : en 5 mois, sur 450.000enfants vaccinés, 250 suppurations importantes, 5adénopathies suppurativesIncidence : 0,6 à 1,2 cas / 1000


BCG : Avis CTV-CSHPF. Mars 2007Levée de l’ obligation vaccinale chez l ’enfant
BCG fortement recommandé ( dès le 1er mois de vie )
- enfant né dans un pays de forte endémie TB- enfant dont l ’un des parents est originaire d ’un de
ces pays- enfant devant séjourner au moins un mois dans l ’un
de ces pays- enfant ayant des antécédents familiaux de TB
( collatéraux ou ascendants directs )- enfants vivant en Ile de France ou en Guyane- enfant jugé par le médecin à risque ( conditions socio-
économiques défavorables - CMU, CMUc, AME -, logement précaire ou surpeuplé )
Tout enfant dont les parents souhaitent la vaccination doit pouvoir être vacciné


PRIORITE ABSOLUE D’UN PLAN NATIONAL DE LUTTE CONTRE LA TUBERCULOSE
Diagnostic précoce des TB-maladie Enquêtes autour des cas contagieux
– Dépistage précoce des TB-maladie– Dépistage précoce des infections TB latentes
Traitements bien conduits et supervisés des TB-maladie Augmentation considérable des prescriptions de traitement préventif des infections TB latentes
– Enfants et adolescents +++– Adultes

ENQUETE AUTOUR D’UN CAS

Quels changements ?
Modifications de la fiche initiale de DO
Création d’une fiche pour la déclaration des issues de traitement (tuberculose maladie)

Modification de la fiche DO
Modifications : des localisations pour mieux repérer les TB respiratoires et les TB extra respiratoires de la question sur profession à caratère sanitaire et sociale
Ajout de questions sur le contexte du diagnostic
Simplification de la partie Bactériologie, suppression des questions sur : préciser le type de prélèvement sur autre technique sur histologie évocatrice
Retrait des questions dépistage et demande d’intervention des services de lutte
antituberculeuse du conseil général


La surveillance des issues de traitement
L’OMS a fixé des objectifs pour les programmes nationaux de lutte anti tuberculeuse: détecter 70% des cas de TB contagieux guérir 85% de ces cas
Indicateur :
% de cas guéris (s’obtient par la surveillance des issues de traitement)


TUBERCULOSES MULTIRESISTANTES