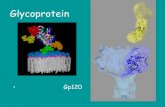
Hépatite virale C les nouveautés en 2011 - collegebvh.org · Hépatite virale C les nouveautés...
Transcript of Hépatite virale C les nouveautés en 2011 - collegebvh.org · Hépatite virale C les nouveautés...

Hépatite virale Cles nouveautés en 2011
F. Lunel FabianiCHU ANGERS
Congrès des biologistes des hôpitauxgénéraux, Angers Septembre 2011

Hépatite virale Cles nouveautés en 2011
Virologie Diagnostic : test Ag, test combiné , ARN Q Traitement : l’aire des trithérapies de 1ère
génération

Cp21
E1gp31
E2gp70
NS2p23
NS3p70
NS4bp27
P7
NS5ap58
NS5bp68
NS4ap8
Capside(site de fixationde l ’ARN viral)
Enveloppe(site de fixation au récepteur
cellulaire)
ARN polyméraseARN dépendante
Sérine-protéase,hélicase, NTPase
Réplication
Modificationspost-traductionnelles
Traduction du brin positif de l’ARN viral
Polyprotéine précurseur du VHC
Co-facteurde NS3
Résistance INF (ISDR,V3)Réplication
Apoptose, cycle cellulaire
C E1 E2 NS2 NS3 NS4 NS55’NC 3’NC
Régions non codantes
Régions structurales
Régions non structurales
Protéines structuralesConstitution de la particule virale
Protéines non structurales
Constitution du complexe de réplication
viroprotéine
Signal peptidases cellulaires
Peptidases virales
Métallo-protéase
Organisation génomique du VHC. (d ’après Moradpour et al., Swiss Med Wkly, 2001)

Variabilité du VHC Production de 1012 particules par jour
Erreur de copie de l’ARN polymérase ARN dépendante, dépourvue d’activité correctrice 5’-3’ exonucléase (103 à 104 substitution par site par an)
Pression de sélection de la réponse immunitaire
Grande diversité: nomenclature 2005 6 génotypes: 1, 2, 3, 4, 5 et 6 Nombreux sous-types: 1 (12), 2 (17), 3 (10), 4 (19), 5 (1), 6 (17) isolat Quasiespèce
Simmonds et al, Hepatology, 2005

5
Epidémiologie
• 3% de la population mondiale infectée(170 millions)
• Cause majeure de cirrhose et de CHC
• 1ère cause de transplantation en Europe

31/10/2011 6
En France
• 0,8 % de la population (évaluation chez 14 000 assurés sociaux)
• 500 000 porteurs chroniques
• 1/3 non encore dépistés

Prévalence du VHC à travers le monde
Afrique 31,9 Millions
5,3%
Europe8,9 Millions
1,03%
Amériques13,1 Millions
1,7%Asie du Sud-Est
32,3 Millions2,15%
Pacifique Occidental62,2 Millions
3,9%
Source OMS 1999: 170 Millions - 3% ; estimation actuelle 200 millions de personnes infectées
Méditerranée Orientale21,3 Millions
4,6%1b1a, 2a, 3a
4a
1a, 1b2, 3
5a
3a -3g
Afrique- Origine 1,2,4,54, 4a2, 5
Europe1a,1b2a, 2b, 3a
Amérique du Sud1a,1b
3a
4
Asie - Origine 3 et 61b, 2a, 2b1a
6a, 7, 8, 9
1b, 3
1b
3a

31/10/2011 8
Cas clinique
Mr X 45 ans Adressé en consultation Bilan sanguin systématique ALAT 90 UI, ASAT 60 UI Sérologie VHC + asymptomatique

31/10/2011 9
Cas clinique
Quel examen réalisez vous en première intention ?

31/10/2011 10
Cas clinique
Quel examen sanguin réalisez vous en première intention ? PCR en temps réel du virus de l’hépatite C

11
ARN du VHC par une technique sensible
Sérologie VHC +
<seuil >seuilInfection par le VHC
nécessitantune prise en charge
spécialisée 70%
Patient ayant guéri
spontanémentlors de son
hépatite aiguë30%

LEGISLATION ACTUELLE
Dépistage : 1 test Confirmation sur un autre prélèvement
test ELISA différent ou immunoblotting Recherche de l’ ARN viral

Diagnostic virologique
Tests indirects (sérologie) :ELISA : mise en évidence d’Ac anti-
VHC ImmunoblotTest combiné Ag/Ac (PMO)
Tests directsAgARN

Benefits of ARCHITECT HCV Ag Assay
25 times more sensitive than previous commercial HCV-Antigen assays: 0.06 pg/mL (3 fmol/L)1 vs. 1.5 pg/mL Ortho TrakC2
Shorter overall processing time than real-time PCR 36 min versus several hours (HCV RNA)
Good correlation with HCV-RNA levels Cheaper than quantitative real-time PCR
1Morota K et al, J Virol Methods 2009;157:8–14.

ARN VHCtechniques récentes
PCR en temps réel : permet de mesurer par fluorescence l’accumulation
des produits d’amplification au cours de la réaction de PCR avec l’aide d’un fluoromètre couplé à un thermocycleur
Plusieurs techniques Abbott HCV real time (12UI/ml, 12 à 100000000
UI/ml) Cobas Taqman Roche HCV (15UI/ml, 43 à 69000000
UI/ml). TMA: Transcription Mediated Amplification: copies d’ARN anti-
sens simple brin avec une T7 RNA polymerase, des primers adéquats en process isotherme

Sérologie Dépistage VHC ELISA Positive confirmée
sur 2ème ELISA
Négative
Négative mais ID ou risque (IVDU, hépatite clinique)
Recherche du Génome VHC
(PCR temps réel: quali + quanti)
Positive Négative
Evaluation de l’atteinte hépatique:
Transa / PBH / Fibroscan / Fibromètre
Indication de traitement?
OUI NON
Absence d’infection ou Guérison
Clinique ou gpe à risque ou cytolyse
Sérologie VHC négative
OU
Algorithme diagnostic de l’infection par le VHC
HEPATITE C DIAGNOSTIC

Infection par le VHC(Sang: Transfusion (avt 1991, toxicomanie, materno-fœtale, nosocomiale,
divers…)
Hépatite aigueSymptomatique pour 20-30% des cas
Guérison (20%)Hépatite résolue (Ac anti-VHC +, ARN -)
Infection chronique (80%)(Ac anti-VHC +, ARN VHC +)
Peu active à très active (Réplication/Lyse cellulaire/Inflammation et Fibrose modérée à extensive)
Cirrhose10 à 20%
Carcinome hépatocellulaire4 à 5% par an
7ème rang des cancers les plus fréquents chez l’homme, très mauvais pronostic
20 à 40 ans
D’après Cheng and Morgan, 2006
Histoire de la maladie

31/10/2011 18
Cas clinique
Toxicomanie IV entre 20 et 30 ans PCR du virus C positive à 6 log d’UI/ml Quels examens biologiques réalisez vous ?

31/10/2011 19
Cas clinique Quels examens biologiques réalisez vous ?
Génotype et quantification du VHC Ag HBs, Ac HBs, Ac HBc, VIH ASAT, ALAT, TP, GGT, PAL, Bili totale EPP TP Marqueurs de fibrose (Fibromètre : Plaquettes, TP, urée, acide
hyaluronique, alpha2 macroglobuline ou Fibrotest APO A1, Haptoglobine, alpha2 macroglobuline, bili, GGT)
Ferritine, % saturation Alpha foetoproteine

31/10/2011 20
Cas clinique
Quel est le but de l’évaluation du clinicien?

31/10/2011 21
Cas clinique n°1
Évaluer si cirrhose ou nonÉvaluer indication de traitement ou nonÉvaluer les chances de r^ponse

Hépatite C chronique :première cause d’hépatopathie grave
Cirrhosesévère
40% 60%
Carcinomehépatocellulaire
30%
Transplantationhépatique
Dans les pays industrialisés, le VHC serait responsable de :
Part relative due au VHC [en % du total]EASL International Consensus Conference on Hepatitis C. Paris, 26-28 February 1999. Consensus statement. J Hepatol 1999 ; 30 : 956-61

Comment évaluer la fibrose ?
- Evaluation directe : biopsie hépatique = « gold standard »
- Evaluation indirecte non invasive (HAS):résultat à interpréter par un spécialiste

Biopsie Hépatique: score METAVIR
F1
F3
F4
F4
F 2

Limites de la Ponction Biopsie Hépatique
Examen invasif Morbidité (0,3%), mortalité (0,03‰) Coût : 1000 € Variabilité
Représentativité de la biopsie hétérogénéité des lésions, longueur de biopsie ( > 20 mm) 1/200 000 è du foie
Observateur Temps Faux négatif pour cirrhose (20%)

Evaluation indirecte non invasive de la Fibrose Scores de fibrose hépatique utilisés en pratique
APRI ASAT, plaquettes
FIB-4 Âge, ASAT, ALAT, plaquettes
Forns Âge, plaquettes, cholestérol, GGT
SHASTA Acide hyaluronique, albumine, ASAT
HépaScore Âge, sexe, bilirubine, GGT,2-macroglobuline, acide hyaluronique
FibroTest Âge, sexe, 2-macroglobuline, haptoglobine,bilirubine, apolipoprotéine A1, GGT
FibroMètre Âge, plaquettes, ASAT, TP, 2-macroglobuline,acide hyaluronique, urée

Fibrometre Résultats des marqueurs
Résultats du FibroMètre
Equivalence Métavir du
FibroMètre : F1
Commentaires du système
expert

Traitement de l’hépatite virale C

EVOLUTION DE L’EFFICACITÉ DES TRAITEMENTS
613
41 3954
63
0
10
20
30
40
50
60
70
IFN24 wk19891
IFN 48 wk19981
IFN+ RBV19981,2
PEG-IFN2000-20023,4,5
PEG-IFN+ RBV
2001-20045,6,7
1. McHutchison et al. N Engl J Med. 1998. 2. Poynard et al. Lancet. 1998. 3. Zeuzem et al.N Engl J Med. 2000. 4. Lindsay et al. Hepatology. 2001. 5. Fried et al. N Engl J Med. 2002.
6. Manns et al. Lancet. 2001. 7. Hadziyannis et al. Ann Intern Med. 2004.
25
*Intent-to-treat analysis

Evolution du taux de RVS chez les naïfs génotype 1
Poynard 1998, McHutchison 1999, Manns 2001,Fried 2002
42
11
36
46
?
7
33
0
10
20
30
40
50
60
70
80
Interferon IFN+Ribavirine PEGIFN+Riba PEG+R+StatC

Génotype 2 or 3 Génotype 1 or 4
PEG IFN 2b 1,5g /sem. Ribavirine 800ouPEG IFN 2a 180g/sem +Ribavirine 800 mg
Pdt 24 semaines
PEG IFN 2b 1,5µg /sem. +Ribavirine 800-1200mg Pdt 48Sem*
(Si G1 HCV< 600.000 UI/ml à J0indetectable à S4 et S12
Pdt 24 sem - AMM 2005)ouPEG IFN 2a 180µg/sem + Ribavirine 1000-1200 mg 48 semaines.*
Traitement de l’hépatite chronique CRecommandations thérapeutiques 2010
*48 sem. si > 2 log à S12 et PCR – à S24

Les profils de réponse virologique
Sustainedresponder
(cure)
Nonresponder
Baseline Treatment
Time
Relapser
Partialresponder
HCV RNAUndetectable
HC
V R
NA
Breakthrough
Detection limit
6 months
Zeuzem et al. N Engl J Med. 2000.

Facteurs préthérapeutiques prédictifs de réponse à la bithérapie pégylée
Facteurs liés aux patients Âge Sexe Ethnie Poids Insulinorésistance Stéatose Statut en vitamine D Dépression Consommation de drogue/d’alcool
Facteurs liés au virus
Génotype Charge virale
(ARN du VHC)
Utiles pour informer les patients sur la probabilité de succès du traitement– L’absence de facteurs favorables n’est pas une contre-indication au traitement
Fibrose/cirrhose Co-infection par le
VIH Génotype de
l’IL28B

LES TENDANCES EN 2011 : L’IMPORTANCE DE LA REPONSE
VIROLOGIQUE PRECOCELES FACTEURS PREDICTIFS

Facteurs prédictifs de RVS
Pré-thérapeutiques Per-thérapeutiques
Choix du traitementBithérapieTrithérapie
Attente
Adaptation thérapeutiqueDurée guidée par la réponse

LE VIRUS : CINETIQUE
Niveau de réplication généralement stable chez lespatients non traités
Valeur prédictive++ des cinétiques de décroissance et denégativation de l ’ARN (M1 et M3) sous traitement
Phase d’induction : inhibition de la réplication virale
Phase de maintenance : élimination des c/ infectéespar le système immun

Taux de réponse virologique prolongée en fonction de la réponse à S4 et S12
Data from (Fried et al) and (Hadziyannis et al).
16%(90/569)
42%(240/569)
22%(128/569)
20%(111/569)
SVR: 87% (78/90) SVR: 5% (5/111)
SVR: 68% (162/240)
<50 IU/mL à S4 (RVR)
>50 IU/mL à S4, <50 IU/mL à S12 (cEVR)>50 IU/mL à S4, >50 IU/mL, but ≥2.0 log reduction à S12 (pEVR)
HCV RNA response:
>50 IU/mL, <2.0 log reduction à S12 (no EVR)
SVR: 73% (240/330)
Peg-IFN alfa-2a (40KD) 180 g/wk plus ribavirin pendant 48 semaines
SVR: 27% (34/128)

Polymorphisme génétique et réponse
IL-28B : 2 SNPs majeurs autour du gène IL-28B associés à la réponse virologique soutenue (RVS) chez les patients traités par interféron/ribavirine genotype 1
Rs12979860 Ge et al. Nature 2009 461 : Tanaka Y et al. Nature Genetics 2009 Rallon et al. AIDS 2010 24 : IV
Rs8099917 Tanaka Y et al. Nature Genetics 2009 41 : 1105 : SNPs au sein
d’une population asiatique Rauch A et al. Gastroenterology 2010 138 : 1338 : Rs8099917
associé à la clairance virale

Poids du polymorphisme IL28B dans la réponse à la bithérapie
McCarthy et al, Gastroenterology 2010Cohorte de 1021 malades
Odds-ratio p
Génotype CC 7,88 0,00005
Génotype 2/3 7,20 0,0003
CV < 600 000 UI/ml 3,58 0,007
Age (ans) 0,92 0,04

Polymorphisme IL28B et cinétique virale
Thompson AJ et al Gastroenterology 2010Semaine 2 4 12
CC
TC
TT
Déc
rois
sanc
e vi
rale
(Log
)0
-1
-2
-3
-4
-5
-6
28% (-)
5% (-)

Poids des facteurs : IL28B versus réponse S4
85%76%
100%
66%
31%
24%
Rép
onse
pro
long
ée (%
)
Thompson et al, Gastroenterology 2010
VPP VPN
CC 69% 68%
S4 (-) 84% 59%
CC CT TT CC CT TT N 115 29 6 291 527 123
ARN – à S4 ARN + à S4

Hépatite C
Nouveaux traitements

PEG + RBVà la carte
Amélioration de moléculesexistantes
Viramidine Albuferon-Telaprevir-Boceprevir- I polyméraseTLR
Inhibiteurs defibrogénèse
2006 2007? 2009 2010 2011
Approches Thérapeutiques Anti-VHC

LES DIFFICULTES
Du fait de la variabilité extrême des protéines NS3 et NS5B en fonction des génotypes, l'efficacité anti-virale des antiviraux, sera variable selon le génotype.
La principale problématique de ces molécules est qu'elles agissent au niveau d'un site moléculaire qui peut muter. Ainsi, les quasi-espèces mutantes seront sélectionnées par les traitements.
Ces phénomènes ont été montrés dans les études cliniques de phase 1 avec des anti-protéases et des inhibiteurs de la polymérase virale.

Les inhibiteurs spécifiques du VHC
McGovern BH et al. Hepatology 2008

Les inhibiteurs de protéase NS3 (1)
EASL 2010 –
Nom Classe thérapeutique Telaprevir (Vx-950) (Janssen,Tibotec)
Inhibiteur protéase NS3/4
Boceprevir (SCH503034) (Schering Plough)
Inhibiteur protéase NS3/4
TMC 435350 (Tibotec Medivir)
Inhibiteur protéase NS3/4
ITMN-191 R7227 (Intermune, Roche)
Inhibiteur protéase NS3/4
BI 201335 (Boehringer)
Inhibiteur protéase NS3/4
MK 7009 (Merck)
Inhibiteur protéase NS3/4
SCH 900518 (Schering Plough)
Inhibiteur protéase NS3
GS-9256(Gilead)
Inhibiteur protéase NS3
Pré-clinique Phase I Phase II Phase III
4,56,57,251, 274,290,754,
757,771.
2016
759
38,749, 753
758,777,
1190
746
N° abstract
2008
?

Les inhibiteurs de protéase NS3 (2)
EASL 2010 –
Nom Classe thérapeutique AVL-181 (Avila)
Inhibiteur protéase NS3
ACH-0141625 (Achillion)
Inhibiteur protéase NS3/4
MK-5172 (Merck)
Inhibiteur protéase NS3/4
BMS-650032 (BMS)
Inhibiteur protéase NS3/4
AVL-192 (Avila)
Inhibiteur protéase
IDX-320(Idenix)
Inhibiteur protéase
Pré-clinique Phase I Phase II Phase III
764
650, 2012
39
761
751
750, 768
N° abstract

RVS (ITT)100
80
60
40
20
0
Patie
nts a
vec AR
N VHC
négatif (%
)
38%
54%a56%b 67%c
75%d
P/R/B 28 sem.(n = 107)
P/R 48 sem.(n = 104)
P/R 4 sem →P/R/B 24 sem.(n = 103)
P/R/B 48 sem.(n = 103)
P/R 4 sem→ P/R/B 44 sem.(n = 103)
Contrôle Sans lead-in28S
Sans lead-in48S
Avec lead-in48S
Avec lead-in28S
EASL 2009 – Kwo P et al. (États-Unis), abstract 4, actualisé
P/R faibledose/B48 sem.(n = 103)
36%
RBV faible dose
ap = 0,013, bp = 0,005, cp < 0,0001, dp < 0,0001 comparé au bras contrôle
Boceprevir: Etude de phase II chez les malades naïfs de génotype 1

PROVE1 : efficacité du telaprevir % RVS
% R
VS
0
20
40
60
80
100
35 %
61 %
41 %
ITT
67 %
Groupe A P/R(48 sem.)n = 80
Groupe B PRT(48 sem.)n = 80
Groupe C(24 sem.)n = 80
Groupe D(12 sem.)n = 20
EASL 2008 – McHutchison - USA, Abstract 4 actualisé
p = 0,001
p = 0,02
31/75 53/79 48/79 6/17

Facteurs prédictifs de réponse à la la trithérapie ?

RVS en fonction du type de non réponse
AASLD 2010 – Bacon BR., États-Unis, Abstract 216 actualisé
72105
77103
PR48 BOC/PR48BOC RGT
29
69 75
0
20
40
60
80
100
RV
S (%
)
5115 23
573058
PR48 BOC/PR48BOC RGT
7
4052
0
20
40
60
80
100
RV
S (%
)
229
Rechuteurs Répondeurs partiels

Cinétiques Virales précoces sous Traitement par Peg-IFN + ribavirine
Dim
inut
ion
de la
CV
(log
cop
ies/
ml)
Pas de réponse (~8%)
>0.5
ETR
0
1
>2.0Réponse
rapide
(~64 %) lente(~24 %)
Réponse
Réponse partielle (4 %)
6mois
LUNEL F, et al J Hepatol. 2003 ; 39 : 826-33Zeuzem et al. J Hepatol 2005;43: 250-257
270 malades naïfsPeg2a 180µg + Riba 1000/1200mg/j

Poordad F, et al. J Hepatol 2011;54(Suppl.):S6
RV
S (%
)
PR48
50/64n/N=
CC TT
BOC44/PR48
44/55
CT
BOC RGT
63/77
PR48
33/116
BOC44/PR48
82/115
BOC RGT
67/103
PR48
10/37
BOC44/PR48
26/44
BOC RGT
23/42
Réalisé chez 653/1048 (62%) des malades inclus dans SPRINT‐2
SPRINT‐2 : RVS en fonction du génotype de IL28B*
78 82 80
28
6571
27
55 59
0
20
40
60
80
100

ADVANCE : RVS en fonction du génotype de IL28B*
Jacobson IM, et al. J Hepatol 2011;54(Suppl.):S542
RV
S (%
)
PR48
35/55n/N=
CC TT
T12PR
45/50
PR48
6/26
T12PR
16/22
PR48
20/80
T12PR
48/68
CT
Réalisé chez 454/1088 (42%) des malades inclus dans ADVANCE
64
90
25
71
23
73
0
20
40
60
80
100

Impact de la fibrose sévère
EASL 2011 – Bruno S., Italie, abstract N°7 actualisé
38 38
22 25
67
41
918
67
52
9 12
0
20
40
60
80
100
F0/1/2 F3/4 F0/1/2 F3/4
%
RVS Rechute
Patients naïfs (SPRINT-2)
PR48 BOC TGR BOC/PR48
Pat
ient
s (%
)
328 24 158 1234 233 1742 231 25319 313n =

226/290 205/279 134/288 24/7345/8545/73
78%73%
47%
62%
53%
33%
F0‐F2 F3‐F4
n/N =0
10
20
30
40
50
60
70
80
90
100
RVS (%
)T12PR T8PR PR
ADVANCE : RVS en fonction du stade de fibrose
Jacobson IM, et al. Hepatology 2010;52(Suppl.):427A

Facteurs prédictifs de la réponse à la trithérapie
• Le bénéfice de la trithérapie chez les malades IL28B CC
parait modeste (Télaprévir) ou absent (Bocéprévir)
• Les facteurs prédictifs sont les mêmes que pour la
bithérapie, mais leur poids est plus faible

Les facteurs per‐thérapeutiques précoces
• Sont-ils identiques à ceux de la bithérapie ?

RESPOND 2 : RVS en fonction de la réponse S8(S4 tithérapie)
AASLD 2010 – Bacon BR., États-Unis, Abstract 216 actualisé
7 8 64 29 74 307 65 74 72 84 70_ _ _ _ _ _
100
86 88
12
40 43
0
20
40
60
80
100
RV
S (%
)
ARN VHC indétectable S8ARN VHC détectable S8
PR 48 BOC RGT BOC/PR48
46 % des patients du bras BOC/RGT sont éligibles pour un traitement de 36 semaines

RESISTANCES

Boceprevir chez les malades non-répondeurs
Profil d’ARN VHC prédisant la survenue de mutation
EASL 2008 – Schiff – USA, Abstract 104 actualisé
Non-répondeursmutations = 49 %
Echappement virologiqueMutations = 82 %
RechuteMutations = 58 %
SuiviSemaines de traitement
LIDRVS
RVS
AR
N V
HC
log
Mutations les plus fréquentes : V36M, T54S, R155K, V36L, V170A, T54A.
Réponse virologique incomplète Non-répondeur
Echappement Rechuteur
0
2
4
6

Alanine (A)
Aspartate(D)
Arginine (R)
A156V/T
Sauvage
Telaprevir1
155 156 168
R155K/T
Boceprevir1,2
36 54
Valine (V)
Threonine (T)
V36A/M T54A
T54A
A156S/V D168A/V/E
A156S/T
170
V170A
ITMN‐1911,3
Valine(V)
1. Kieffer TL, et al. Hepatology. 2007;46:631. 2. Tong X, et al. Antiviral Res. 2006;70:28. 3. Seiwert S, 1st International Workshop on Hepatitis C: Resistance and New Compounds. October 25‐26, 2006. Graphic courtesy of Dr. Ira M. Jacobson.
54
Résistance in Vitro aux anti-protéases

Qu’en sera-t-il demain?
L'hypothèse la plus vraisemblable est que la base du traitement restera fondée sur l'association Interféron Alpha et Ribavirine, les inhibiteurs spécifiques du VHC sont proposés en trithérapie dans la nouvelle AMM.
Dans tous les cas, le caractère durable de la réponse dans l'hépatite chronique C et les nombreuses approches thérapeutiques nouvelles notamment les optimisations de traitement incitent à l'optimisme.

Merci!

Facteurs prédictifs : analyse multivariée
P <0.0001
BOC/PR48 vs PR48
BOC/RGT vs PR48
P = 0.002
P <0.0001
P <0.001
Only covariates remaining significant at α=0.05 after adjustment for the other variables were retained in the model as shown in the figure. Factors entered but not retained in the model were, region, race, gender, weight, BMI, steatosis, platelets, ALT, statin use, and fibrosis
Baseline HCV-RNA:≤400,000 vs. >400,000
IL28B Genotype: CC vs. Non-CC
Age ≤40 vs >40
Genotype: 1b/Other vs 1a
P <0.0001
P <0.0001
23
Only 7-9% of patients had VL ≤400,000