Les lésions échographiques...
Transcript of Les lésions échographiques...
La paroi vasculaire
Epaisseur et structure variables
artère/veine
type d’artère
3 tuniques concentriques Intima : endothélium /sous endothélium /L.E.I
Média : fibres musculaires lisses , élastiques
et collagènes / L.E.E
Adventice : tissu conjonctif
Importance des réglages (F, résolution, profondeur)
Mesures possibles, entre interfaces et non I/M/A +++
Calibre veineux variable
- selon le volume contenu dans la veine
- selon de la position (veines des MI, veines jugulaires)
- En temps réel, l’échographie peut montrer un discret
glissement systolique longitudinal du liseré externe
par rapport aux tissus environnants
- Le mouvement de la paroi artérielle est dominé par la
pulsatilité radiale de l’artère témoignant du passage de
l’onde de pouls
La paroi artérielle normale
Aspect échographique des vaisseaux
Principes d’analyse identiques quel que soit
le territoire et le type de vaisseau
Étude de la paroi
Étude du contenu
Étude de l’environnement
La paroi artérielle normale
E.I.M (ou I.M.T ) Mesurable de façon simple et non invasive sur les artères
superficielles
Critère important dans études épidémiologiques, en
recherche clinique
!! standardisation des mesures: analyse semi-automatique
Analyse densitométrique des niveaux de gris sur une
longueur >1cm: précision >1/10mm
La paroi artérielle normale
Liseré interne
= Interface
sang / intima
Intermédiaire anéchogène
Liseré externe hyperéchogène
= Inteface média / adventice
Lumière
Interface sang-intima
Interface média-adventice
Tissus péri-vasculaires
Optimisation des réglages 2D
Paroi artérielle normale
2D: Incidence perpendiculaire
Imagerie de flux : vérification (possible lésion anéchogène)
La paroi artérielle normale
Valeur normale ACC: 0,5 à 0,7mm
(abaques / âge-sexe-ethnie)
ASE 2008; 21
Cerebrovasc Dis 2009; 27
Bien visible sur la plupart des artères
avec sondes de hautes fréquences
Limite = ne peut dissocier I/M
Intérêt des mesures semi-automatiques
ACC: segment de référence, 2 cm
sous la bifurcation , segment rectiligne,
versant postérieur / faisceau US
Calcifications dans la paroi artérielle
Images en pointillés hyperéchogènes au sein de la paroi
Lésions diffuses
Médiacalcose
Les lésions athéromateuses
Lésions focales
Distribution anatomique
Siège : artères de gros et moyen calibre
Sites privilégiés (facteurs hémodynamiques) :
segments proximaux, bifurcations et boucles
Territoires indemnes: membres supérieurs
Prédominance face postérieure des artères
Genèse et progression de la plaque vers la sténose
Phénomène très lent
Initiation de la plaque
Croissance
Genèse et progression de la plaque vers la sténose
Remodelage artériel
Développement de la plaque dans la paroi initialement compensé par une augmentation du volume du vaisseau
La lumière reste normale … pendant un temps limité
Bien visible en échographie
- Dysfonction endothéliale entrée du LDLc sanguin
dans la paroi artérielle oxydation du LDLc ,
devient cytotoxique pour l’endothélium
- L’endothélium lésé va favoriser le recrutement
de monocytes qui vont capter le LDLc oxydé et se
transformer en macrophages puis en cellules spumeuses
Mécanismes de la maladie athéromateuse
- Les macrophages vont entretenir une réaction
inflammatoire au sein de la plaque et sécréter des
métalloprotéases qui peuvent être à l’origine
de la rupture de plaque
- Les cellules musculaires lisses migrent de la
média vers l’intima, se multiplient et sécrètent du collagène
et de la matrice extra-cellulaire, qui vont former la chape
fibreuse de la plaque
- Le LDLc va également s’accumuler dans
le milieu extracellulaire puis se regrouper
au sein d’un “noyau lipidique”
Mécanismes de la maladie athéromateuse
Morphologie
normale
Complications Épaississement Plaque
Anomalies
morphologiques
Genèse et progression de la plaque
Erosion ou rupture de plaque
cicatrisation
Thrombus
thrombolyse physiologique ou
incorporation dans la plaque
Occlusion
suppléance par circulation collatérale
Ischémie aiguë
Lésion silencieuse
symptomatique
Cycle évolutif des plaques
IV
ou V
VI
Instabilité
Rupture
VI
Thrombus
Hématome
Progression V Cicatrisation
Facteurs favorisant la rupture
Facteurs extrinsèques: HTA, effort, stress…
Facteurs intrinsèques: vulnérabilité de la plaque
composition relative en lipides et en tissu fibreux
contraintes mécaniques
solidité de la chape fibreuse
Caractéristiques échographiques des lésions / Corrélations avec histologie
Anéchogène ou hypo-échogène
Dépôts lipidiques confluents
Hémorragie
Nécrose
Echogène, Hyperéchogène
Fibrose
Ombre acoustique
Calcification
Analyse échographique des lésions
Plaques d’athérome : structure focale
d’épaisseur >1.5 mm ou différence > 0.5 mm
ou 50% /EIM adjacente (consensus 2004)
Analyse
Dimensions et disposition
Echogénicité
Echostructure
Surface
Plaques d’athérome: dimensions
Plusieurs coupes dans différents plans
Mesure : longueur, épaisseur
Disposition : excentrée ou circonférentielle
Situation / repères anatomiques (bifurcations
artérielles)
Coupe transverse / Coupe longitudinale Un seul plan de coupe: surévaluation ou sous-estimation de la sténose
Plaques d’athérome: échogénicité
Echelle de gris en 2D
Définition par rapport à des références
Anéchogène : sang circulant
Isoéchogène : muscle
Hyperéchogène : structures osseuses
Hypoéchogène : niveau intermédiaire
« Ulcération » Anfractuosité >2mm de profondeur et de longueur
fond bien identifié/paroi artérielle (à différencier de
deux plaques contiguës)
niche circulante (flux lent !! PRF et réglages)
Classification de Nicolaïdes
Type 1 : plaques anéchogènes
Type 2 : plaques à dominance hypoéchogène (> 50%) avec de petites zones échogènes
Type 3 : plaques à dominance échogène (> 50%) avec de petites zones hypoéchogènes
Type 4 : lésions uniformément isoéchogènes ou hyperéchogènes
Type 5 : lésions inclassables, artéfact d’ombre acoustique
Nicolaïdes 1995, adaptation de la classification de Gray Weale 1988
Evènements inflammatoires :
dilatation vasa vasorum existants et
néo angiogenèse
Lien entre bio marqueurs spécifiques
des facteurs inflammatoires au sein
de la plaque et degré de
vascularisation
Hyper vascularisation et instabilité de la plaque
En pratique
Toute plaque présente un risque d’embolisation
Ce risque est d’autant plus important que
Plaque de > 50% volume anéchogène ou hypoéchogène
Surface anfractueuse ou ulcérée
Chape fibreuse absente (tout ou partie)
Présence de néovaisseaux
Artérite inflammatoire
Groupe hétérogène de maladies
Atteinte inflammatoire des vaisseaux intéressant aussi bien l’endothélium que la média ou même l’adventice
Sténoses ou occlusions
Aspect échographique
Spécificités
Epaississement hypo ou isoéchogène
Epaississement souvent circonférentiel et étendu
Localisations particulières / maladie en cause
Absence d’athérome (!! association possible)
Sténoses segmentaires, souvent effilées et régulières, rares anévrysmes
Artérite radique
Contexte: souvent doses élevées et à distance
Lésions souvent isoéchogènes
Quand suivi systématique à 10 ans: jusque 40% de lésions significatives STEELE Am J Surg 2004
Localisations peuvent différer de l’athérome
liées à la zone d’irradiation
facilement bilatérales HALAK Eur J Endovasc Surg 2002
Evolution dépend aussi des FRCV associés
!! Examen parfois difficile en raison des
remaniements tissulaires péri artériels (cou radique)
Penser à prendre sonde de plus basse fréquence
Aspect le plus souvent homogène
Lésions souvent bilatérales
Clivage de la paroi artérielle par un hématome spontané ou secondaire à
une brèche intimale
Dissections sous-intimales (A,B): sténosantes, responsables d‘AI
hémodynamique ou embolique
Dissections sous-adventicielles (C,D): peuvent évoluer vers un anévrisme
Double chenal artériel possible dans les 2 cas
Flap intimal mobile dans la lumière très rare
La dissection de la paroi artérielle
Anomalies de calibre et longueur
1, 2 : Tortuosité ou
flexuosité en forme
de S ou de C
3, 4 : Coiling ou
enroulement
5 : Kinking ou
plicature sténosante
Anomalies de calibre et longueur
Anévrysmes
Dilatation artérielle ou veineuse
Thrombose
Signes échographiques d’évolutivité
Faux anévrysmes : pas de paroi propre
iatrogènes
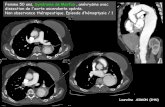
Anévrysme de l’aorte abdominale
L’échographie de contraste permet de délimiter parfaitement les
contours du sac et de la partie circulante
Evaluation du risque de rupture
Aspect du thrombus:
hétérogénéité avec
zones anéchogènes
ou hypoéchogènes
Aspect de la paroi:
soufflure, contours mal
définis
Faux anévrysme
Evaluer les vitesses au collet
Modifier la PRF pour évaluer la partie circulante
Flux typique: inversion du sens circulatoire entre systole et diastole
Lumière artérielle normalement anéchogène
Artefacts (échos de répétition )
à partir de la paroi la plus superficielle / sonde
Les anomalies intra-luminales
Stase dans la lumière
Echos fins mobiles, rare dans les artères
Thrombose :
Thrombus cruorique: sur plaque, aspect
variable selon l’âge, +/- occlusif
Embole: amas échogène endoluminal souple,
contexte clinique
Membrane de dissection
Endartérectomie (TEA) : aspect normal
Disparition de la plaque et du liseré pariétal interne Limite de la TEA souvent visible « en marche
d’escalier » Aspect parfois soufflé (dilatation segmentaire)
Pontages veineux
Saphène interne in situ (dévalvulation, ligature des perforantes) ou saphène interne inversée (valvules en iso courant) ou saphène externe
Paroi mince, bourgeons intra luminaux éventuels (résidus valvules)
Artérialisation progressive de la paroi
Pontages prothétiques
Prothèses annelées en Dacron: pointillés
obliques des mailles
Prothèse en PTFE (Gore Tex): aspect en
rail (double liseré)
Types d’anastomose
Termino-terminales, latéro-terminales
ou termino-latérales
Avec ou sans patch d’élargissement
Diversité des lésions et des possibilités
de revascularisation: compte-rendu
opératoire indispensable
Contrôle précoce
Vérification de la perméabilité du montage
et de l’amélioration des flux d’aval
Recherche des erreurs techniques: sténose
anastomotique, valvule résiduelle, FAV (SI
in situ, perforante), plicature quand excès
de longueur, plicature ou occlusion
positionnelle quand traversée articulaire
Suivi des pontages
Pontages veineux: hyperplasie pariétale
anastomotique ou diffuse, sténose sur
valvule, irrégularités de calibre avec zones
anévrismales, récidive athérome
Prothèses: hyperplasie +/- sténose aux
anastomoses, thrombus pariétal
Stents
Pointillés hyperéchogènes endoluminaux
Aspect variable selon le matériau utilisé
Contrôle du flux dans le stent et aux
extrémités
Contrôle du lit d’aval
Complications
Hyperplasie intimale diffuse ou localisée, simple ou sténosante
Thrombus, thrombose
Plicature, rupture localisée
Endofuite de type II à partir d’une A. Lombaire. Mécanisme et extension
facilement analysables en échographie de contraste, complémentarité des 2
plans de coupe et apport du Doppler couleur et pulsé
Endofuite de type 1: diagnostic 2D Nouveau contrôle à J14 après reprise et pose d’un stent
Injection de contraste pour s’assurer de l’absence d’endofuite résiduelle