Institut de Génomique Fonctionnelle, France · La cellule saine ... - Génération de cellules...
Transcript of Institut de Génomique Fonctionnelle, France · La cellule saine ... - Génération de cellules...

Institut de Génomique Fonctionnelle, France INSERM U1191, CNRS 5203, Université de Montpellier
Dalle Stéphane, Directeur de Recherche, INSERM
DIPLOME d’UNIVERSITE MEDECINE REGENERATRICE
Ilots de Langerhans, cellules et cellules souches pancréatiques
Comment élaborer/remplacer les cellules pancréatiques ? Enjeux et problématiques ?

Introduction
How to make -cells ?
« Significant challenges remain for each strategies: First, it is important to set the bar high
with respect to requirement for newly generated cells:
properly regulated insulin secretion and the capacity of cell renewal (replication)
are at the top of the list…»
D’après Borowiak, M., Melton DA, Curr Opinion Cell Biology, 2009, 21, 727-732

Plan
La cellule saine
« Comprendre pour mieux appréhender les problématiques »
- Son environnement
- Comment définir une cellule saine
- Origine et cycle de vie
La cellule malade: Diabètes
« Comprendre pour mieux appréhender les enjeux »
- Problématique pour le diabète de type 1
- Problématique pour le diabète de type 2
La cellule réparée:
« Cellules souches et stratégies »
- Stratégies actuelles et perspectives
- Génération de cellules endocrines à partir de cellules immatures (cellules ES et iPS)
- Régénération des cellules au sein du pancréas

Rappels anatomiques: Le pancréas et l’architecture de l’îlot
Corps
du pancréas
Queue
du pancréas
Canaux
interlobulaires
Canal pancréatique
de Wirsung
Canal biliaire
Bile
Duodénum
Plis
circulaires
Abouchement
ampoule de Vater
Ampoule de Vater
Canaux
interlobulaires Flux enzymes digestives
vers le duodenum
Cellules acineuses
Réseaux capillaires
Cellules
Cellules
Cellules
Îlot de Langerhans
(1%)
Canal
lobulaire
Adapté d’après © Encyclopædia Britannica, Inc.
Pancréas in situ
Pancréas
Cellules canalaires

Rappels anatomiques/histologiques: Architecture de l’îlot de Langerhans
Foie Estomac
Pancréas
Intestin
Pancréas
Duodénum
Îlot de
Langerhans
Cellule(s) exocrine(s)
Zymogène
Capsule
Capillaires
Cellule Cellule Cellule
Proinsuline
Insuline Peptide-c Glucagon Somatostatine
Localisation des cellules pancréatiques dans les îlots de Langerhans Adapté d’après Expert Reviews in Molecular Medicine © Cambridge University Press
Interactions endocrine-exocrine
Interactions intercellulaires

Rôle de la cellule pancréatique: Sécrétion d’insuline et homéostasie glucidique
Pancréas Îlot
de Langerhans
Cellule
Insuline
Vx
sanguins
Glucose
Fibres musculaires
Plateforme histologie (IGF, Montpellier)
Microscopie électronique (CRIC, Montpellier)
Dr S. Costes, Dr C. Broca

La cellule saine
« Comprendre pour mieux appréhender les problématiques »
- Son environnement
- Comment définir une cellule saine
- Son cycle de vie
La cellule malade: Diabètes
« Comprendre pour mieux appréhender les enjeux »
- Problématique pour le diabète de type 1
- Problématique pour le diabète de type 2
La cellule réparée:
« Cellules souches et stratégies »
- Stratégies actuelles et perspectives
- Génération de cellules endocrines à partir de cellules immatures (cellules ES et iPS)
- Régénération des cellules au sein du pancréas

Phase 1:
- rapide et activée par
[Ca2+] locale
- mobilisation du pool
de granules conditionnés
(pool RRP)(n < 100/cellule)
L’exocytose est biphasique

Mécanismes d’activation par le glucose: Initiateur/déclencheur
Cellule pancréatique Dalle S et al. J Biol Chem (1999) 274:10869
K+
MITOCHONDRIE
RE
Membrane plasmique
G6P
Pyr
Glucose
Ca2+
1
Ca2+
2 3
Ca2+
ext
int
Insuline (+ C-peptide)
SERCA 3
Mitochondrial
transport
VDCC
CC / IP3R
KIR 6.2
Glut 2
Cycle de Krebs
Equivalents réduits
Chaine respiratoire
ATP
Ashcroft FM, Rorsman P. Cell (2012) 148, 1160
Henquin JC. Diabetologia (2009) 52, 739

La cellule saine
« Comprendre pour mieux appréhender les problématiques »
- Son environnement
- Comment définir une cellule saine
- Son cycle de vie
La cellule malade: Diabètes
« Comprendre pour mieux appréhender les enjeux »
- Problématique pour le diabète de type 1
- Problématique pour le diabète de type 2
La cellule réparée:
« Cellules souches et stratégies »
- Stratégies actuelles et perspectives
- Génération de cellules endocrines à partir de cellules immatures (cellules ES et iPS)
- Régénération des cellules au sein du pancréas

Masse des cellules pancréatiques adultes et renouvellement
Croissance/Néogenèse Mort
CELLULES SOUCHES
PROGENITEURS
PROGENITEURS
Canaux pancréatiques

Equilibre dynamique
Masse fonctionnelle de cellules
Néogenèse
- Progéniteurs canaux pancréatiques
- Transdifferenciation
- Progéniteurs intra-îlots
Plasticité de l’îlot de Langerhans
Senescence/Vieillissement
- Facteurs génétiques
- Stress oxydant
- Détérioration de l’ADN
Replication
A partir de cellules préexistantes - Importante chez le fœtus
- Réduite chez l’adulte
Apoptose
Vie et mort des cellules pancréatiques

Développement postnatal
Gestation
Obésité
Régimes Hypergluc/Hyperlip
Insulinorésistance
Régénération
Fonction
Masse
Fonction
Masse
Autoimmunité inflammation
Vieillissement
Glucotoxicité/lipotoxicité
Programmation in utéro (malnutrition)
Facteurs cytotoxiques
La plasticité de la masse permet d’adapter au long cours la fourniture en insuline
aux besoins métaboliques de l’organisme
Quand la robustesse de ces adaptations est dépassée…
l’hyperglycémie s’installe: DT1, DT2
Phénomène de compensation par les cellules pancréatiques

Prentki, M. et al. J. Clin. Invest, 2006, 116, 1802-1812
Phénomène de compensation par les cellules pancréatiques

TGF-, Activine A
EGF (NGF, VEGF, FGF), IGF-1
Hormones/incretines
GH, GLP-1
REPLICATION et
DIFFERENCIATION
+ -
Pancreatic cells
APOPTOSE
NEOGENESIS
DIFFERENCIATION
Cellules precurseurs +
SENESCENCE
-
INGAP (Ilotropin)
Nutriments
Glucose, FFA
Nutriments
Haut Glucose, FFA
Cytokine
Facteurs Inflammation
IL-1, TNF-, IL-6,
Interféron
Facteurs stress oxydant
Altération ADN
+ + + + + +
EGF, IGF-1 GLP-1
Facteurs controlant la différenciation et la masse des cellules pancréatiques

PROLIFERATION
Cellules pancréatiques
APOPTOSE
DIFFERENCIATION +
+ -
CRIC-Montpellier
Haut glucose (hyperglycémie)
Diabète de type 2
Glucose
(concentrations physiologiques)
Régulation de la masse des cellules pancréatiques (plasticité) :
Dualité des effets du glucose

La cellule saine
« Comprendre pour mieux appréhender les problématiques »
- Son environnement
- Comment définir une cellule saine
- Son cycle de vie
La cellule malade: Diabètes
« Comprendre pour mieux appréhender les enjeux »
- Problématique pour le diabète de type 1
- Problématique pour le diabète de type 2
La cellule réparée:
« Cellules souches et stratégies »
- Stratégies actuelles et perspectives
- Génération de cellules endocrines à partir de cellules immatures (cellules ES et iPS)
- Régénération des cellules au sein du pancréas

Role central des cellules pancréatiques dans le DIABETE
Diabète de type 1 (10% des sujets diabétiques)
Destruction des cellules par un processus autoimmun
Carence totale en insuline : Injections
Insuline = seule hormone hypoglycémiante de l’organisme
Diabète de type 1 et type 2 : Déficit de l’insulino-sécrétion
Diabète de type 2 (90% des sujets diabétiques)
Déficit sécrétoire et mort par apoptose des cellules ,
associés à une résistance à l’action de l’insuline
Carence partielle puis totale en insuline: Arsenal thérapeutique
Hyperglycémie chronique
Complications dégénératives du diabète

Proposed model for the different pathways contributing to the execution of cytokine-induced ß-cell apoptosis. Arrows indicate genes for which expression was modified by cytokines in a time course microarray analysis. ß-Cell apoptosis is probably mediated by
three main pathways—namely JNK, ER stress, and liberation of pro-apoptotic proteins from the mitochondria.
Apoptose des cellules pancréatiques et diabète de type 1
Cnop, M. et al. Diabetes, 2006, 54S2, 97-107

Les enjeux pour le diabète de type 1, et de type 2
Préserver Restaurer
Diabète de type 2
(Dysfonction cellule )
Agents pharmacologiques
Diabète de type 1
(Perte cellule )
Transplantation Pancréas entier/ Ilots de Langerhans
Thérapie cellulaire (?)
une masse fonctionnelle
de cellules
Recherches fondamentale et clinique

ND
DT2
Butler, A.E. et al. Diabetes, 2003, 52, 102-110 Del Guerra, S. et al. Diabetes, 2005, 54, 727-735
« cell deficit and increased cell apoptosis in humans with type 2 diabetes »
« Therapeutic approaches designed to arrest cell apoptosis could be a significant new development
in the management of type 2 diabetes »
Cellules pancréatiques et diabète de type 2

Adapté de Primary Care, 26, Ramlo-Halsted BA, Edelman SV, The natural history of type 2 diabetes. Implications for clinical practice, 771–
789, © 1999, with permission from Elsevier.
Développement et progression du diabète de type 2 et de ses complicationsa
(représentation conceptuelle)
Progression du diabète de type 2
Insulino résistance
Fonction cellulaire
Insulinémie
Glucose post-prandial
Glycémie à jeun
complications macrovasculaires
complications microvasculaires
Intolérance au glucose Diagnostic du diabète
4-7 années

Préserver la fonction et la survie des cellules est essentiel
Importance des études sur le maintien et/ou la restauration de la masse
des cellules fonctionnelles chez les diabétiques de type 2
Déclin de la sécrétion d’insuline et de la masse de cellules
Hyperglycémie chronique
Intérêt de prendre en charge tôt le pancréas
- Cibler les fonctions physiologiques du pancréas
- Agir sur l’insuline (et le glucagon)
- Maintenir la structure de l’îlot: Masse fonctionnelle de cellules pancréatiques
Les enjeux pour le diabète de type 2

La cellule saine
« Comprendre pour mieux appréhender les problématiques »
- Son environnement
- Comment définir une cellule saine
- Son cycle de vie
La cellule malade: Diabètes
« Comprendre pour mieux appréhender les enjeux »
- Problématique pour le diabète de type 1
- Problématique pour le diabète de type 2
La cellule réparée:
« Cellules souches et stratégies »
- Stratégies actuelles et perspectives
- Génération de cellules endocrines à partir de cellules immatures (cellules ES et iPS)
- Régénération des cellules au sein du pancréas

Stratégies actuelles
D’après Borowiak, M., Melton DA, Curr Opinion Cell Biology, 2009, 21, 727-732

Stratégies actuelles: Quelles sources de cellules (à partir de 2011) ?

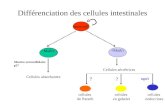
Génération de cellules endocrines à partir de cellules immatures

Rappels d’embryogénèse: Origine et développement des cellules pancréatiques

Facteurs de transcription impliqués dans la différenciation pancréatique

Cellules ES: Différenciation en cellules produisant de l’insuline Cellules$ES:$Différencia4on$en$cellules$
produisant$de$l insuline$
Cellule%ES%Précurseur%endodermal%
Cellule%insuline%+%
D amour,(Nature(biotech,(2005,(2006(
Cellules ES Précurseur endodermal Cellule Insuline +
D’amour, Nature Biotech, 2005, 2006

could also be seen from another angle. Indeed, retinoidsignalingwasshowntoactivateBMPexpression inseveralin vivo and in vitro systems including embryonal carci-noma cells and differentiating mouse embryoid bodies(34–36). It isnot yet clear whether this inductiveeffect onBMPalso occursduringhEScell differentiation. Neverthe-less, considering the in vivo function of BMPsignaling inthe midgut endoderm, it appears reasonable that bothretinoid signaling and BMP antagonism were required inthesestudiesfor stronginductionof apancreatic fatefromtheDEcellswhilepreventinghepatic differentiation. How-ever, it is likely that theeffect of RA iscontext-dependentbecausewhenapplied onhES-derived DEcellscultured atlow density, it resulted in the inhibition of Smad 1/5/8phosphorylation (23). It remains to beelucidated whetherthis later effect representsan artifact of in vitro cultureoraspecific retinoid effect at the single cell level.
Other studies made use of RA combined with FGFligands(FGF4, FGF7, FGF10) or of Noggin combined withFGF2and EGFto inducepancreatic cellsalbeit at alowerefficiency than for combined Noggin and RA (Table 3)(13,14,16,17,19,23). Our unpublished observations suggestthat FGF signals favor hepatic gene expression in theabsence of BMP antagonism, but the addition of FGFligands together with BMP antagonism (Noggin) and RAenhances pancreatic gene expression. Furthermore, theinduction of PDX1 cells by combined Noggin and RArequires at least a basal level of FGF activity (via theextracellular signal–regulated kinase/mitogen-activatedprotein kinase [ERK/MAPK] pathway [Fig. 3]) given thatthe addition of the MAPK-inhibitor U1026 prevented pan-creatic cell differentiation (20). Because RA is known to
act synergistically with FGF signaling during endodermpatterning, supplemented FGF can be seen as an enhanc-ing factor in protocols that already integrate Noggin andRA (13,14,19). This view might resolve the nature offactors X suggested as involved in the indirect effects ofRA in Xenopus dorsal endoderm (37). It was recentlysuggested that in thepresenceof FGF7, RAcan efficientlyinduce PDX1 progenitors from hES-derived DE cellsseeded at low density (5–50,000 cells/cm2) and that thiseffect is paralleled by inhibition of Smad1/5/8 phosphory-lation, thereforerecapitulatingBMPantagonismdescribedabove (23).
Recent analysis of the signaling network during earlyliver and pancreas development in 3–6 somites-stagemouse embryos further indicated that inhibition of theactivin signaling significantly increases the proportion ofcells fated toward PDX1expression. Thesefindings there-fore suggest that the addition of activin inhibitors to theabove-mentioned cocktails might still boost the occur-rence of PDX1 cells in hEScell cultures (13,24).
Despite the fact that combining BMP antagonism withretinoid signaling efficiently generates PDX1 pancreaticprogenitors from hES-derived definitive endoderm, therequirement for hedgehog antagonism with cyclopamineduring pancreas induction from these cells has not beenclarified by thesestudies. Theinitial report byD’Amour etal. (18) indicated the necessity to antagonize hedgehogsignaling that is indeed activated during EScell differen-tiation, and it was shown to also play a negative role exvivo by limiting endocrine and exocrine genes expressionin embryonic (E12.5) mouse pancreatic explants (38,39).However, additional studies using Noggin, FGF ligands,
TABLE 3Derivation of PDX1 progenitors from hEScells
References DE induction Pancreas induction Differentiation Key features
D’Amour (2006) ActA Wnt3a; ActAFBS
FGF10 Cyclo (4d);FGF10 Cyclo RA(4d)
DAPT Ex4; IGF1HGF Ex4
7%INS cells, doubleendocrine cells; no glucoseresponse
Johannesson(2009)
ActA Wnt3a; ActAFBS
FGF4 RA ( / Cyclo) — 32%PDX1 cells, very low INSexpression
Cai (2009) ActA; ActA ITS (DE replating on 3T3)FGF7 RA (6d)
HGF Ex4 NA(6d)
90%PDX1 ; co-expressionFOXA2, HNF1b, HNF4a,HNF6, NKX6.1; some INScells
Jiang (2007) ActA NaBut (7d) EGF bFGF NG(14d);EGF NG(7d)
NA IGF2 (5d); NA(2d)
EBs after DE induction; buddingPDX1 INS clusters; 3D isbetter
Kroon (2008) ActA Wnt3a; ActAFBS
FGF7 (4d); NG RAFGF7 (4d)
Transplantation inimmunodeficientmice
Endocrine cells in grafts,glucose response in vivo at 3months, protection from STZeffect
Vallier (2009) ActA BMP4 bFGF(3d)
NG RA FGF10SB431542 (6d)
— PDX1 clusters, culture infeeder-free settings
Zhang (2009) ActA Wortmanin(4d)
NG RA FGF7 (4d);EGF (5d)
bFGF Ex4 BMP4NA ITS(7d)
20%PDX1 , 25%INS , lowglucose response, ITSissuenot addressed
Mfopou (2010) ActA Wnt3a; ActAFBS
NG RA Cyclo (8d);FGF10 Ex4Compound E (4d)
NA Ex4 IGF1BMP4
50–80%PDX1 in 4 hESlines,co-expression FOXA2, SOX9,HNF1b, HNF6, NKX6.1, lowPTF1a. Some INS cells
Recent models of pancreas differentiation from hEScells integrate BMP antagonism and retinoid signaling early after definitive endoderminduction. This allows for concomitant hepatic blockade and pancreas induction from definitive endoderm cells. Cyclo, cyclopamine;DAPT, N-[N-(3,5-Difluorophenacetyl)-L-alanyl]-S-phenylglycine t-butyl ester (gamma secretase inhibitor); EBs, embryoid bodies; Ex4,exendin-4; FBS, fetal bovine serum; ITS, insulin selenium transferring supplement; NA, nicotinamide; NaBut, sodium butyrate; NG, Noggin;STZ, streptozotocin; 3D, three dimensional. The text in bold marks protocol with combination of NGand RA.
J.K. MFOPOU AND ASSOCIATES
diabetes.diabetesjournals.org DIABETES, VOL. 59, SEPTEMBER 2010 2097
Cellules$ES:$Différencia4on$en$cellules$produisant$de$l insuline$
Mfopou,(diabetes(2010(
Cellules ES: Différenciation en cellules produisant de l’insuline
Mfopou, Diabetes, 2010

Cellules iPS: Différenciation en cellules produisant de l’insuline iPS$cells:$Différencia4on$en$cellules$produisant$du$CRpep4de$et$de$l’insuline$
www.cell-research.com | Cell Research
Donghui Zhang et al.
431
npg
Day 0
HumanES cells
Endoderminduction
Pancreaticspecialization
Progenitorexpansion Maturation
Act A+Wort
DF12 DF12F12/IMDM
EGF
DMEM
Nico+bFGF+Ex-4+BMP4Insulin-
producing cells
4 8 13 20
0 4 8 12 16 20
0 4 8 12 16 20
0 4 8 12 16 20
0 4 8 12 16 20
1.0
0.4
1.0
0.4
1.0
0.4
1.0
0.4
Re
lative
ge
ne
expre
ssio
nR
ela
tive
gen
e e
xp
ressio
n
Rela
tive g
ene e
xp
ressio
nR
ela
tive g
ene e
xpre
ssio
n
Sox17 T Foxa2 Oct4
Pdx1 Hnf6
Pax4 Pax6
MafA Glut2
Nkx6-1 Tcf1
Insulin Glucokinase
0.0%
0.3%
96.4%
25.3%
Forward scatter
Sox17
CX
CR
4In
su
lin
100 10
1 10
2 10
3 10
4
10
0
1
01
1
02
1
03
10
4
10
0
10
1
1
02
10
3
10
4
10
0
10
1
10
2
1
03
10
41
00
10
1
1
02
10
3
1
04
100 10
1 10
2 10
3 10
4
100 10
1 10
2 10
3 10
4
100 10
1 10
2 10
3 10
4
SOX17 DAPI
Insulin DAPI
A
B
D
F
G
C
E
RA+NOGGIN+FGF7
Time (day) Time (day)
Time (day) Time (day)
iPS$cells$
Fibroblaste$humain$
Cell Research | Vol 19 No 4 | April 2009
H ighly effic
i
en t gen erat ion of ins ul in-producing cel ls
436
npg
MafA Glut2
Pdx1 Insulin
C1 C2 C5 H9
Re
lative
ge
ne
exp
ressio
n
3
2
1
0
C1
C5
C2
H9
D4 SOX17 D8 PDX1 D13 SOX9
D20 Amylase
C-peptidePDX1
D20 PDX1 D20 Insulin
A
C
D
B
PDX1 C-peptide PDX1 C-peptide DAPI
Cell Research | Vol 19 No 4 | April 2009
H ighly effic
i
en t gen erat ion of ins ul in-produci ng cel ls
436
npg
MafA Glut2
Pdx1 Insulin
C1 C2 C5 H9
Rela
tive
ge
ne e
xp
ressio
n
3
2
1
0
C1
C5
C2
H9
D4 SOX17 D8 PDX1 D13 SOX9
D20 Amylase
C-peptidePDX1
D20 PDX1 D20 Insulin
A
C
D
B
PDX1 C-peptide PDX1 C-peptide DAPI
!$25%$de$cellules$produisant$de$l’insuline$à$par4r$de$cellules$ES$et$iPS$
Zhang(Cell(research(2009(
Zhang, Cell Research, 2009
25% de cellules produisant de l’insuline à partir de cellules ES et iPS
Fibroblaste humain
iPS cells

Limites à l’utilisation de cellules pluripotentes
Ethique ?
Finesse des protocoles de différenciation à mettre en place:
Utilisation de molécules spécifiques, en associations complexes,
fenêtres d’action courtes, cultures 3D (Wandzioch, Science 2009)
Risque tératogène des cellules pluripotentes
Risque spécifique des iPS:
Mutations de séquences codant pour des protéines, anomalies épigénétiques…
Tumorigénèse possible (Gore, Nature 2001; Lister Nature 2001)

Régénération cellulaire au sein du pancréas
Physiologique chez le sujet obèse ou la femme enceinte
Quelles sont les cellules à l’origine de cette régénération ?

Régénération des cellules au sein du pancréas ?

Preuve de concept

Preuve de concept

Régénération des cellules pancréatiques (1)

Régénération des cellules pancréatiques (2)
Bibliographie sélectionnée Dor, Nature 2004 Xu, Cell 2008 Nir, J Clin Invest 2007 Collombat, Cell 2009 Thorel, Nature 2010 Herrera, Nature 2010

Régénération cellulaire au sein du pancréas: Limites
Origines du renouvellement β-cellulaire débattues
Etudes in vivo chez le rongeur uniquement
Quelles molécules pharmacologiques pour promouvoir cette régénération ?
- A partir de canaux: Tumorigénèse ?
- A partir de cellules α ou β: dysfonction endocrine / dosage/rapport cellulaire ?

Conclusion
How to make -cells ?
« We believe that the potential of cellular therapies for diabetics is ever closer
and is an achievable goal…»
D’après Borowiak, M., Melton DA, Curr Opinion Cell Biology, 2009
Les progrès effectués ces 10 dernières années
permettent d’envisager de nouvelles sources pour traiter le patient diabétique
- Cellules pluripotentes
- Cellules reprogrammées
- Cellules régénérées in situ
Avantages sur transplantation îlots ou pancréas
- Contrôle qualité
- Masse infusée contrôlée et adaptée
- Greffe autologue
Autres voies de recherche parallèles
- Lutte contre l’auto-immunité
- Site alternatif de transplantation (Ilots), tolérance…
- Autres encore non explorées ?

Institut de Génomique Fonctionnelle, Montpellier, France INSERM U1191, CNRS 5203, Université de Montpellier
Merci pour votre attention

INSTITUT de GENOMIQUE FONCTIONNELLE
Physiopathologie de la Cellule Pancréatique
INSERM U661 – UMR CNRS 5203 – Universités Montpellier 1 et 2
INSTITUT de RECHERCHE en BIOTHERAPIE
Laboratoire de thérapie cellulaire du Diabète
CHU Montpellier
DIPLOME UNIVERSITAIRE MEDECINE REGENERATRICE
Ilots de Langerhans,
cellules et cellules souches pancréatiques
Merci pour votre attention

îlots de Langerhans
Pancréas
Anatomie du pancréas
Bloc duodéno-hépato-pancréatique Adapté d’après © sanofi-aventis France
Foie Veine Porte Vésicule Biliaire Canal Cystique Canal Hépatique Canal Cholédoque Artère Hépatique Rein droit Ampoule de Vater Tête du pancréas Canal de Wirsung
Veine cave inférieure
Aorte
Diaphragme Artère gastrique Tronc coeliaque Glande surrénale Artère et veine spléniques Rate Queue du pancréas Corps du pancréas Rein gauche Jéjunum Artère et veine mésentériques sup Duodénum Veine mésentérique