Reconnaissance des microorganismes par les molécules et ......Reconnaissance innée Dr. Isabelle...
Transcript of Reconnaissance des microorganismes par les molécules et ......Reconnaissance innée Dr. Isabelle...
Reconnaissance innée
Dr. Isabelle CREMER MCU Université Paris 6 U872 INSERM, équipe 13: « Microenvironnement Immunitaire et Tumeurs » Centre de Recherche des Cordeliers. 75006 Paris E-mail: [email protected] Novembre 2010
Reconnaissance des microorganismes par les molécules et les cellules du système
immunitaire
Plan du cours
Barrières anatomiques
Barrières physiologiques
Reconnaissance par les cellules du système immunitaire:
Les cellules tueuses naturelles NK, lymphocytes Tγδ
Les cellules phagocytaires
Reconnaissance par les molécules du système immunitaire:
Les récepteurs Toll-like « TLR »
Les lectines de type C Les récepteurs « scavengers » (poubelles)
Introduction
Réponse à une première infection: 3 phases
Immunobiology (Janeway et al.)
Immunité adaptative plus tardive. Temps d’expansion clonale des LT et LB spécifiques du pathogène.
Comparaison entre immunité innée et adaptative
D’après McGuinness D.H. et al. 2003. Trends in Parsitology 19:312
Barrières anatomiques
A. La peau (épiderme/derme)
B. Les muqueuses (conjonctive/tractus digestif, respiratoire, génito-urinaire)
- Epiderme: Cellules épithéliales étroitement associées, couche kératinisée - Derme: tissu conjonctif/vaisseaux sanguins/follicules pileux/glandes sébacées et sudoripares - La barrière mécanique retarde l’entrée des micro-organismes - L’environnement acide (pH 3-5) retarde la croissance des micro-organismes
- Rôle protecteur de la salive/larmes/sécrétions muqueuses - Le mucus sécrété par les cellules épithéliales enrobe les micro-organismes étrangers - Les cils (voies respiratoires et tractus gastro-intestinal) rejettent les micro-organismes vers l’extérieur
Barrières physiologiques
A. La température
B. Le pH
C. Les médiateurs chimiques
- La température corporelle normale inhibe la croissance de certains pathogènes - La fièvre inhibe la croissance de certains pathogènes
- L’acidité du contenu stomacal tue la plupart des micro-organismes ingérés
- Le lysosyme (sécrétions) clive la paroi cellulaire (peptidoglycane) des bactéries - L’interféron induit un état antiviral dans les cellules - Le système du complément lyse les micro-organismes ou facilite la phagocytose
Reconnaissance par les cellules du système immunitaire:
- Les cellules phagocytaires
- Polynucléaires - Macrophages - Cellules dendritiques
- Cellules cytotoxiques
- Natural Killer (NK), - Lymphocytes Tγδ
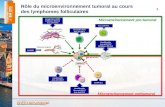
Reconnaissance des micro-organismes par les cellules de l’immunité innée
A. Les cellules phagocytaires
1. Les polynucléaires
- Passent dans le sang - Collés à l’endothélium - Fonction de phagocytose - Durée de vie courte:24 h - Ne se divisent pas - Noyau multilobé - Granulation caractéristique neutrophile éosinophile basophile
2. Les macrophages
- Cellules fortement adhérentes - Issus des monocytes du sang - Localisés dans les tissus (Histiocytes des tissus conjonctifs, macrophages alvéolaires du poumon cellules de Kupffer dans le foie macrophages des ganglions et de la rate) - Durée de vie longue: 1 à 3 mois
2. Les macrophages: fonctions
- Grosses granulations cytoplasmiques:enzymes - Récepteurs membranaires
- CR1 et CR3 pour le C3b - RFcγ pour les IgG - Rfcε pour les IgE - Pour les Interférons
- Sécrétion de cytokines - Sécrétion de protéines plasmatiques:
- C1 à C5, facteur B et D, properdine, facteurs de la coagulation.
Granules contiennent des enzymes (lysosyme, myéloperoxydase, élastase…) et des peptides antimicrobiens (défensines)
- Phagocytose (Metchnikoff, 1883): Les macrophages sont les premières cellules à reconnaître les microorganismes dans les tissus. Les polynucléaires sont normalement présents dans le sang. Suite à une infection, ils sont recrutés dans les tissus.
2. Les macrophages: cytokines sécrétées en réponse aux produits bactériens
(Immunobiology Janeway et al.)
(d’après Randolph G. et al. Nat. Rev. Immunol. 2005)
3. Cellules dendritiques de la peau
Cellules de Langerhans
Cellules dendritiques dermiques
Application de fluorescéine sur la peau induit inflammation, et migration des DC dans les ganglions drainants (fluorescence verte)
Tissu périphérique (peau, muqueuse)
3. Fonctions des cellules dendritiques
pathogène DC im
Cellule dendritique immature
- Endocytose (forte expression de PRR)
- Réponse aux cytokines inflammatoires
- Faible capacité de présentation antigénique
DC m
T
T
T
Cellule dendritique mature:
- Faible endocytose (faible expression de PRR)
- Réponse aux chimiokines homéostatiques
- Forte capacité de présentation antigénique (forte expression de molécules du CMH, molécules de costimulation
Organes lymphoïdes secondaires
B. Les cellules Natural Killer (NK)
- Ce ne sont pas des cellules spécifiques: - Pas de double restriction Ag/CMH sur la cellule cible - Pas de récepteur des cellules T (TCR)
- Cytotoxicité: - Sécrétion de perforine - Sécrétion d’IFNγ - Sécrétion de TNFα - Induction de l’apoptose
- Présence de marqueurs communs avec les T cytotoxiques:
- Récepteur au Fc de Ig - Récepteur à l’IFN, IL-1, IL-2
Reconnaissance par les molécules du système immunitaire:
Reconnaissance des PAMPs par les PRR
1) Reconnaissance TLR-PAMPs 2) Transduction d’un signal intracellulaire 3) Sécrétion des cytokines pro-inflammatoires tels que le TNFα, l’Il-1 et l’Il-6.
Les composants microbiens reconnus
Les PAMPs ont 3 caractéristiques communes qui font d’eux des cibles idéales pour l’immunité innée:
1) Ils sont produits uniquement par les micro-organismes, et pas par les cellules du soi.
Ceci permet une distinction entre le « soi » et le « non soi » infectieux
2) Ils sont invariants entre les micro-organismes d’une classe donnée. Ceci permet qu’un nombre limité de « PRR » détecte la présence d’une
infection microbienne. (exemple: le lipide A du LPS étant très conservé, toutes les bactéries Gram- seront détectées)
3) Ils sont essentiels pour la survie des micro-organismes. Des mutations ou la perte d’un PAMP sont létales, ou diminuent leur capacité d ’adaptation; des mutants d’échappement à la réponse immunitaire ne pourront être générés.
Les PAMPs
Les PAMPs sont: - le LPS de la paroi des bactéries Gram -, - le peptidoglycane et l’acide lipotéichoïque de la paroi des bactéries Gram + - le sucre mannose (commun dans les glycolipides et les glycoprotéines microbiens mis rares dans les cellules humaines) - le N-formylméthionine trouvé dans les protéines bactériennes - l’ARN double brin des virus - le β-glucane des parois fongiques - les motifs CpG d’ADN bactérien - la flageline, la piline - les lipoprotéines
Les PAMPs peuvent également être reconnus par des récepteurs solubles circulant dans le sang qui fonctionnent comme des opsonines et initient les voies d’activation du complément.
Il est supposé que le système de l’immunité innée peut reconnaître environ 103 structures moléculaires différentes.
Les récepteurs de l’immunité innée (1)
D’après McGuinness D.H. et al. 2003. Trends in Parasitology 19:312
1. Les lectines de type C
Famille de protéines qui lient des résidus glucidiques spécifiques sur des glycoprotéines ou des glycolipides. Certaines lectines comme la PHA ou la conA sont mitogéniques.
Les lectines de type C sont des lectines membranaires caractérisées par un domaine de reconnaissance des carbohydrates (CRD : « Carbohydrates Recognition Domain »). Le CRD interagit avec des glycoprotéines possédant un mannose ou un galactose, et cette interaction est dépendante du Ca2+.
Elle sont exprimées essentiellement par les macrophages et les cellules dendritiques. Elles induisent la phagocytose et la présentation antigénique.
Membres de cette famille: Dectine (récepteur au β-glucan) MMR « mannose macrophage receptor » (endocytose) DC-SIGN Dec 205 (endocytose)
Dectine (récepteur au β-glucan)
Zymosan: particule insoluble de la paroi des champignons dont le b-glucane est un des composants.
β-glucan: polymères de glucose composants majeurs de la paroi de la plupart des champignons, (certaines plantes et bactéries).
La dectine possède un motif ITAM dans sa partie cytoplasmique, qui est phosphorylé après fixation du β-glucane.
D’après Brown G. D. et al. 2003. Immunity 19:311
MMR « mannose macrophage receptor »
MMR: Récepteur d’endocytose. Contient plusieurs domaines de liaison des carbohydrates.
Il fixe des oligosaccharides avec différentes affinités: mannose = fucose > Nacétylglucosamine = glucose.
Ces ligands sont présents sur des bactéries, champignons, cellules infectées par des virus et parasites.
Après fixation du ligand sur ce récepteur, le micro-organisme est phagocyté, et le récepteur recyclé à la surface cellulaire.
2. Les récepteurs « scavengers »
- Famille de 3 classes de récepteurs membranaires multi-domaines: SR-A, SR-B et SR-C. Pas de structure commune aux 3 classes
- Liaison à des ligands polyanioniques et à des lipoprotéines de faible densité
- Récepteurs exprimés par les cellules myéloïdes (macrophages et cellules dendritiques) et certaines cellules endothéliales
- Rôle dans la clearance des corps apoptotiques
- Rôle dans la fixation et la phagocytose des micro-organismes
-Rôle dans le métabolisme lipidique
3. Les récepteurs du complément
Récepteur Ligand Expression Fonction
CR1/CD35
CR2/CD21
CR3/Mac-1/ CD11b
CR4/CD11c
C3b,C4b Macrophages, monocytes, polynucléaires Lymphocyte T et B
Phagocytose, clairance des complexes immuns,
C3d,C3dg Lymphocyte B Corécepteur de l’activation B, récepteur de l’EBV
C3bi, ICAM-1 Micro-organismes
Macrophages, monocytes, NK, neutrophiles
Phagocytose
C3bi Macrophages, monocytes, NK, neutrophiles
Phagocytose
4. Les récepteurs « Toll-like »
Toll est un gène de drosophile essentiel pour l’ontogénèse et la résistance antimicrobiennne.
Plusieurs homologues de Toll ont été identifiés et clonés dans les vertébrés et ont été nommés les « Toll-like receptors » (TLR).
La famille des récepteurs « Toll-like » comprend des protéines transmembranaires phylogénétiquement conservées qui sont essentielles pour l’immunité innée.
Caractéristiques des TLR
1) Les TLR sont une famille de récepteurs transmembranaires
2) 10 récepteurs ont été identifiés chez les mammifères ayant des fonctions distinctes dans la reconnaissance des PAMPs
3) Les TLR reconnaissent souvent plusieurs ligands différents
4) Certains ligands ne sont toujours pas identifiés
5) Certains TLR requièrent des protéines accessoires pour reconnaître leur ligand
Structure des récepteurs de la famille IL-1R/TLR
Domaine cytoplasmique TIR: Toll/Interleukin-1R domain. Domaine d’interaction protéine/protéine
Domaine TIR
Domaines « Ig-like »
Domaine répété riche en leucine LRR « Leucine Rich Repeat »
IL1-R IL-18R
Toll TLR1 à 10 MyD88 et TIRAP
Adaptateurs moléculaire
Les récepteurs « Toll-like » des cellules de mammifères, et leurs ligands
D’après Medzhitov R. et al. 2001. Nature Rev. Immunol. 1:135
TLR4 - 1er récepteur Toll caractérisé chez l’homme
- Exprimé par plusieurs types cellulaires dont les macrophages et les cellules dendritiques
- Fonctionne comme un récepteur de transduction du signal pour le LPS
- Plusieurs molécules accessoires requises: LBP (« LPS Binding Protein) CD14 (récepteur de forte affinité pour le LPS) soluble ou ancré dans la membrane MD-2: petite protéine dépourvue de région transmembranaire et exprimée à la surface cellulaire en association avec TLR4.