La Lettre de linfectiologue Daclatasvir-asunaprévir et inhibiteur de NS5B (BMS791325) dans les GT1...
-
Upload
adrienne-bertin -
Category
Documents
-
view
104 -
download
1
Transcript of La Lettre de linfectiologue Daclatasvir-asunaprévir et inhibiteur de NS5B (BMS791325) dans les GT1...

La Lettre de l’infectiologue
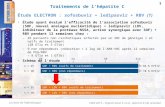
Daclatasvir-asunaprévir et inhibiteur de NS5B (BMS791325) dans les GT1 (1)
• Essai randomisé contrôlé multicentrique ouvert de phase IIb– Daclatasvir = inhibiteur du complexe de réplication NS5A à activité
pangénotypique– Asuprénavir = antiprotéase NS3 avec activité antivirale contre les virus
de génotype 1,4,5 et 6
• 12 semaines de traitement sans interféron
• Stratification sur sous-type GT1a/1b et présence d’une cirrhose confirmée par biopsie (10 % par groupe)
CROI 2014 – D'après Hawkins T et al., abstract 25, actualisé
DCV 30 mg x 2/j + ASV 200 mg x 2/j + BMS-791325 75 mg x 2/j
DCV 30 mg x 2/j + ASV 200 mg x 2/j + BMS-791325 150 mg x 2/j
12 semaines de suiviSuiviadditonnelde 48 sem.
n = 80
n = 86
J0 S12 S24
Critère principal RVS12

La Lettre de l’infectiologue
Fin de traitement RVS4 RVS120
20
40
60
80
100 97.592.4 92.294.2 91.7 91.7
Ré
po
ns
e, p
ou
rce
nta
ge
de
pa
tie
nts
Daclatasvir-asunaprévir et inhibiteur de NS5B (BMS791325) dans les GT1 (2)
Critère principal (RVS12) - cas observés
CROI 2014 – D'après Hawkins T et al., abstract 25, actualisé
2
DCV + ASV + ‘325 75 mg DCV + ASV + ‘325 150 mg
78/80 81/86 73/79 77/84 71/77 77/84
Données manquantes en post-traitement à S12
DCV + ASV + ‘325 75 mg DCV + ASV + ‘325 150 mg
3 patients, ITTm RVS12 = 88,8 % 2 patients, ITTm RVS12 = 89,5 %

La Lettre de l’infectiologue
Daclatasvir-asunaprévir et inhibiteur de NS5B (BMS791325) dans les GT1 (3)
Réponse au traitement (RVS12) dans les différentssous-groupes
CROI 2014 – D'après Hawkins T et al., abstract 25, actualisé
3
Cirrhotiq
ues
Non- cirr
hotiques
GT 1
a
GT 1
b
IL-2
8b CC
IL-2
8b
n
o...0
20
40
60
80
100100
91 91100
9691
71
94 91 94 9689
Pa
tie
nts
RV
S1
2 (
%)
DCV + ASV + ‘325 75 mg DCV + ASV + ‘325 150 mg
8/8 5/7 63/69 72/77 59/65 62/68 12/12 15/16 23/24 27/28 48/53 50/56

La Lettre de l’infectiologue
Daclatasvir-asunaprévir et inhibiteur de NS5B (BMS791325) dans les GT1 : une combinaison orale prometteuse (4)
• Pas de différence entre les 2 dosages 75 et 150 mg (75 mg avec combinaison à dose fixe choisi pour les études de phase III UNITY 1 et 2)
• Peu d’échecs virologiques (tous GT1a)
• Les patients GT1b avec polymorphisme NS3 ou NS5A (n = 7)ont tous présenté une RVS
• La présence de mutations initiales associées à une résistance(NS3, NS5A ou NS5B) n’est pas prédictive de la survenue d’un échec virologique
• Bonne tolérance – très peu d’arrêts de traitement pour EI (n = 2)
Conclusions
CROI 2014 – D'après Hawkins T et al., abstract 25, actualisé
➜ Traitement sans IFN et RBV efficace avec plus de 90 % de RVS malgré une proportion élevée de patients cirrhotiques (38 %de F3-F4 prouvée par biopsie), GT1a (82 %) et IL28B non-CC