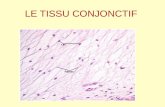
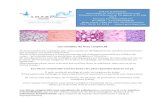
Lymphome B centrofolliculaire cutané primitif : à distinguer
Étude pratique du tissu conjonctif lâche sous-cutané chez la souris
Transcript of Étude pratique du tissu conjonctif lâche sous-cutané chez la souris
Étude pratique du tissu conjonctif lâche sous-cutané chez la souris
F. BAZIN ( Maître de Conférences en Biologie)
M.H. BESLIER (technicienne de laboratoire de Biologie)
1°) Principe de la technique de la « boule d’oedème ».• Le tissu conjonctif a la propriété de retenir l’eau en gonflant (formation d’un œdème), si le drainage assuré normalement par la circulation lymphatique est insuffisant.• La technique utilisée est celle de la « boule d’œdème » modifiée d’après la technique initiale due à RANVIER.• Le principe de cette technique est de provoquer un oedème localisé en injectant dans un tissu conjonctif d’accès facile, une solution contenant un colorant. Du formol est ajouté à la solution pour conserver les cellules et faciliter leur coloration.La solution injectée a ainsi une triple action :
Faire gonfler le tissu conjonctif, écarter ses constituants et permettre le prélèvement de fragments translucides observables sous le microscope.
Colorer les cellules dispersées dans la préparation et les organes inclus dans ce tissu.Conserver le mieux possible la structure et la composition des constituants du tissu, ce que l’on
désigne en Histologie par la « fixation ».• L’étude de cellules contenant des lipides demande l’emploi de colorants particuliers, solubles dans les lipides et dans les solvants des lipides. Des solutions colorées d’éthanol peuvent être utilisées bien qu’elles ne permettent pas de réaliser un véritable œdème.
2°) L’observation des préparationsDes fragments d’œdème colorés seront montés entre lame et lamelle pour être observés sous le microscope.
• L’épaisseur des préparations sera relativement forte par rapport à celle des coupes (5μm) des préparations microscopiques classiques faites pour l’étude histologique des tissus et des organes.
• Le microscope peut être utilisé pour observer des préparations épaisses, si elles sont suffisamment transparentes. La difficulté réside dans la faible épaisseur de préparation fournissant une image nette pour un objectif donné : la « profondeur de champ ». Plus l’objectif donne un fort grossissement, plus faible est cette profondeur de champ.
• Les observations se feront progressivement en utilisant en premier un objectif X10, puis X40. Les objectifs X100 à immersion ont une profondeur de champ très faible qui limite l’observation à la surface de la préparation. Les objectifs x100 et X50 à immersion peuvent être utilisés à condition d’immobiliser la lamelle en la bordant de vernis (lutage de la lamelle).
3°) Préparation de la souris• La souris, de préférence mâle, doit être choisie la moins grasse possible. Les femelles multipares ayant beaucoup de tissu adipeux sous-cutané ne doivent pas être utilisées.
• Les souris de race blanche permettent une meilleure observation de la coloration des boules d’œdème.
•La manipulation se fait sur un animal mort, mais encore chaud et souple. La souris est euthanasiées par asphyxie et immédiatement fixée par les pattes sur une plaquette de liège.
1: mouiller le poil et le coiffer pour dégager une ligne de peau nue
2: couper la peau sur la ligne dégagée
3: décoller le volet de peau en déchirant le tissu conjonctif lâche sous-cutané et le fixer avec des épingles.-
1
2
Préparation d’un volet de peau pour la confection des boules d’oedèmeAttention : essuyer très soigneusement pinces et ciseaux après section de la peau pour retirer les poils qui y adhèrent. Les poils sectionnés se collent facilement sur le conjonctif mis à nu.
Face interne de la peau présentant une surface de tissu conjonctif collante : ne pas la toucher avec les doigts, ne pas la laisser sécher.
3
La confection des boules d’œdème par injection de liquide coloré
seringue
support
épaisseur de la peau
Piquer l’aiguille en la faufilant dans le tissu conjonctif, seringue tenue tangentiellement à la peau
Injecter la solution colorée
« cloque » de la boule d’oedème
Injecter la solution colorée jusqu’à ce que la boule d’œdème mesure 10mm de diamètre
pinces finesciseaux fins
Prélever la boule d’œdème en la tenant avec les pinces fines
Deux boules d’œdème, avant leur
prélèvement. Après
Injections d’une solution
de bleu de méthylène
abdomen
veines
Face interne de
la peau
Montage entre lame et lamelle de la boule d’oedème
1) Poser la boule d’œdème au centre de la lame porte-objet parfaitement sèche
Sans frotter ni faire glisser sur le verre
pinces
lame de verre porte-objet
Lame porte-objet vue de profil
2) Grande lamelle couvre objet posée àsec
3) Introduire de la solution colorée sous la lamelle
La tension superficielle de la solution exerce une pression suffisante de la lamelle pour aplanir la boule d’oedème
Observation d’ensemble de la préparation à faible grossissement
A, A’ : tissu conjonctif lâche. Choisir les plages les plus claires pour une observation à plus fort grossissement.
B : tissu conjonctif adipeux
C : veine et vaisseaux capillaires. Les artères et artérioles sont moins visibles.
D : section de nerf. L’aspect ondulé est du au prélèvement de la boule d’œdème.
E : faisceau de fibres musculaires striées (en cas de prélèvement large, proche de la musculature abdominale).
F : portion de glande mammaire englobée dans le tissu adipeux (utilisation d’une souris femelle).
Boule d’œdème obtenue par injection de solution formolée de bleu de méthylène
Les fibroblastes
Fibres de collagène entrecroisées
Fibroblaste
Boule d’oedème colorée par le bleu de méthylène(observation à l’objectif x40)
Cytoplasme faiblement basophile
Noyau volumineux avec amas nucléolaire
Long prolongement cytoplasmique entrecroisé avec les fibres de collagène non colorées
Fibroblaste coloré par le bleu de méthylène
( observation à l’objectif x100 ih )
Les adipocytes
Fibres de collagène entrecroisées
Boule d’oedème colorée par le bleu de méthylène(observation à l’objectif x40)
Adipocytes isolés
gouttelettes lipidiques
noyau
Les adipocytes groupés forment un tissu conjonctif particulier : le tissu adipeux
Coloration par le bleu de méthylène Coloration des lipides par le noir soudan
noyaunoyau
Les lipides accumulés repoussent cytoplasme et noyau en périphérie de cellules pressées les unes contre les autres.
Les mastocytes
Fibres de collagène entrecroisées
emplacement du noyau (non coloré)
granules cytoplasmiques métachromatiques
granules dispersés hors de la cellule
noyau
amas nucléolaire
Le bleu de méthylène colore en mauve (métachromasie) les granules des mastocytes intactes. Tout le colorant entrant dans la cellule est capté par ces granules. Le noyau n’est visible que par son image en « négatif ».
Les mastocytes peuvent éclater au cours de la confection des préparations. Ils présentent des images de « dégranulation »mimant la dégranulation de ces cellules à l’occasion de réactions allergiques. Le bleu de méthylène peut accéder au noyau et le colorer.(observation : objectif X100 ih.)
Granulocytes, Monocytes, Macrophages et Histiocytes
Monocyte : noyau réniforme Macrophage : vacuole de phagocytose (*)
1
2
Ganulocytes (pseudo-)éosinophiles caractéristiques des rongeurs
1) Coloration du noyau par le bleu de méthylène
2) Coloration des granulations éosinophiles : boule d’œdème colorée par une solution aqueuse d’éosine.
Granulocyte neutrophile coloré par le bleu de méthylène
Histiocytes : grandes cellules àcytoplasme vacuolisé et noyau central, dotées de capacités d’athrocytose (cf. : diapo. Tissu conjonctif inflammatoire)
Observations : objectif X100 ih.
*
Les vaisseaux sanguins (*) et les nerfs sont entourés de tissu conjonctif
(*) Les vaisseaux lymphatiques également (cf. diaporama : mise en évidence des vaisseaux lymphatiques)
hématies
Veinule entourée d’adipocytes : *Vaisseau capillaire, nerfs et veinule
nerf
nerf veinule
**
granulocyte
Vaisseau capillaireFibres de collagène et fibroblastes
hématiesNoyau de cellule endothéliale
Nerf
Ceci n’est ni un nerf ni un vaisseau !
Segment de poil de souris collé sur la boule d’oedème
Noyau de cellule de Schwann
Faisceau de fibres nerveuses = cylindraxes
Réaction inflammatoire du tissu conjonctif sous-cutané
• Des souris mâles placées dans une même cage se battent fréquemment et se mordent, ce qui entraîne une inflammation de la peau autour des morsures et plus en profondeur, dans le tissu conjonctif sous-cutané.
• Une inflammation comparable peut être provoquée par une injection sous-cutanée de carmin lithiné (1). La fabrication des boules d’œdème s’opère 24h après l’injection comme pour un tissu normal.
Noyau de fibroblaste1
2
Granulocyte neutrophile
Histiocytes
Les cytoplasmes sont chargés de granules rouges de carmin lithinéabsorbés par athrocytose
1 : macrophage avec une vacuole de phagocytose contenant un granulocyte
2 : boule d’œdème dans du tissu conjonctif sous-cutané après injection de carmin lithiné. Coloration des noyaux par le bleu de méthylène.
(1) Le carmin lithiné est confectionné suivant la méthode décrite dans GABE (in « Techniques Histologiques » p.827-828, Masson et Cie édit. 1968).
Fibres de collagène