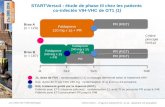
Étude LEAGUE-1 : daclatasvir + simeprevir ± RBV dans les GT1 (1)
description
Transcript of Étude LEAGUE-1 : daclatasvir + simeprevir ± RBV dans les GT1 (1)

La Lettre de l’infectiologue
Étude LEAGUE-1 : daclatasvir + simeprevir± RBV dans les GT1 (1)
• DCV 30 mg x 1/j (dose réduite) + SMV 150 mg x 1/j + RBV fonction du poids– Dans cette étude, les concentrations en DCV dues à la co-administration
avec SMV étaient plus basses que prévu
Étude de phase II randomisée en ouvert
CROI 2014 – D'après Hézode C et al., abstract 28LB, actualisé
J1 S12 S48
Re-randomisation à S12 (1:1)
GT1bNaïfs (n = 104)Répondeursnuls (n = 43)
GT1a(exploratoire)
1:1
Ran
dom
isat
ion
Naïfs(n = 12)
RépondeursNuls
(n = 9)
S24
DCV + SMV12 semaines
(n = 76)
36 semaines de suivi
24 semaines de suiviDCV + SMV12 semaines
36 semaines de suivi
24 semaines de suivi
DCV + SMV + RBV12 semaines
(n = 71) DCV + SMV + RBV12 semaines
24 semaines de suiviDCV + SMV + RBV24 semaines
24 semaines de suiviDCV + SMV + RBV24 semaines

La Lettre de l’infectiologue
S4 (RVR) Fin de traitement
RVS12 S4 (RVR) Fin de traitement
RVS120
20
40
60
80
100 7991 85
6574
656982 75
8595 95
Patie
nts
avec
ARN
du
VHC
indé
tect
able
(%)
Naïfs
42/53
35/51
48/53
42/51
45/53
38/51
15/23
17/20
Répondeurs nuls
17/23
19/20
15/23
19/20
Étude LEAGUE-1 : daclatasvir + simeprevir± RBV dans les GT1 (2)
Efficacité pour les GT 1b
CROI 2014 – D'après Hézode C. et al., abstract 28LB, actualisé
DCV + SMVDCV + SMV + RBV
Analyse en ITT
RVS12 “as observed” n/N (%) DCV + SMV DCV + SMV + RVB
Données manquantes en post-traitement à S12
exclues
Naïfs 45/50 (90) 38/46 (83)
Répondeurs nuls 15/19 (79) 19/20 (95)

La Lettre de l’infectiologue
Étude LEAGUE-1 : daclatasvir + simeprevir± RBV dans les GT1 (3)
RVS12 en fonction de la durée de traitement pour les GT1b
CROI 2014 – D'après Hézode C et al., abstract 28LB, actualisé
DCV + SMV DCV + SMV + RBV
DCV + SMV DCV + SMV + RBV
0
20
40
60
80
10081 75
83
10089
74
50
89
RVS1
2 IP
W (%
)±
IC80
Naïfs Répondeurs nuls
DCV + SMV 12 semainesDCV + SMV 24 semainesDCV + SMV + RBV 12 semainesDCV + SMV + RBV 24 semaines
RVS12“as observed”
n/N (%) DCV + SMV DCV + SMV + RVB
12 semaines 24 semaines 12 semaines 24 semaines
Inclutles patients
re-randomisésà S12
Naïfs 20/22 (91) 24/24 (100) 20/23 (87) 18/21 (86)
Répondeurs nuls 9/9 (100) 6/10 (60) 11/11 (100) 8/9 (89)

La Lettre de l’infectiologue
Étude LEAGUE-1 : daclatasvir + simeprevir± RBV dans les GT1 (4)
• Patients naïfs– RVS12 chez 67 % (8/12) des patients
Incluant 2/2 patients cirrhotiques et 6/10 non cirrhotiques Échec virologique chez 33 % (4/12) des patients
• Répondeurs nuls– Possibilité de bénéficier de l’addition de PR après que 5 patients
aient présenté un échec virologique (7 patients au total)– 9/9 patients : absence de RVS
Efficacité pour les GT1a
➜ Cette association DCV 30 mg + SMV 150 mg ± RBV a permis d’obtenirdes taux de RVS12 de 75 à 85 % chez les patients naïfs et de 65 à 95 %chez les répondeurs nuls dans les GT 1b
➜ La tolérance a été bonne (hyperbilirubinémies de grade ¾ liées à la RBV)➜ La dose de 60 mg pour le DCV est celle retenue pour les essais futurs –
y compris ceux incluant le SMV
CROI 2014 – D'après Hézode C. et al., abstract 28LB, actualisé