CHAP O-1 : Stéréochimie - Chimie !ckapota.pagesperso-orange.fr/PCSI/DS-DM/stereochimie...III-...
Transcript of CHAP O-1 : Stéréochimie - Chimie !ckapota.pagesperso-orange.fr/PCSI/DS-DM/stereochimie...III-...
CHAP O-1 : Stéréochimie
I- Présentation des molécules
II- Modes de représentation spatiale des
molécules
III- Conformations : analyse conformationnelle
IV- Configurations
V- Isomérie optique : propriétés des isomères de
configuration
1
A- Introduction • Ecriture :
• Formule brute
• Formule développée
• Formule semi développée
• Forme topologique
• Nomenclature
• Nombre d’insaturations (liaisons π ou cycles) nI
pour un composé de formule brute CxHyOzNvXw le nombre
d’insaturations ou cycles vaut :
• Ex : C6H6 O ni=
2
22 wvyxni
I- Présentation des molécules
2
B- Isomérie
Définition : deux isomères sont deux corps différents de même formule brute. 1. l’isomérie de constitution ou plane :
formule brute identique, formule développée différente
Il y a plusieurs types d’isomères de constitution : de chaine, de position, de fonction.
2. la stéréoisomérie ou isomérie spatiale : Formule brute identique, formule développée identique
la différence provient uniquement de l’arrangement des atomes dans l’espace :
STEREOCHIMIE.
Rappel : il y a libre rotation autours d’une simple liaison
Pas de libre rotation autour d’une double liaison
a- stéréoisomères de conformation : conformères
isomères conformationnels : stéréoisomères obtenus par simple rotation autours de
liaisons simples
b- stéréoisomérie de configuration :
Isomères de configurations : ceux qui ne sont pas des conformères
Conséquence : pour passer d’une configuration à une autre il est nécessaire de
casser au moins deux liaisons. 3
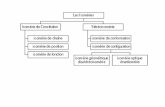
C- Résumé
OUI
IMPOSSIBLE !!!
ISOMERES
Même formule brute CxHyOzNvXw
Nombre d’insaturations et de cycles
ISOMERES de CONSTITUTION STEREOISOMERES
Même formule Semi développée
NON OUI
Images l’un de l’autre dans un miroir
Même chaîne carbonée
NON OUI
ISOMERES de CHAINE Même position des fonctions
NON OUI
ISOMERES de POSITION Même fonctions
NON
ISOMERES de FONCTION
ENANTIOMERES DIASTEREOISOMERES
NON OUI
Superposables par rotation autour des liaisons simples
STEREOISOMERES de
CONFIGURATION
STEREOISOMERES de
CONFORMATION
NON OUI
4
H4
H5H6
H1
C1 C2
H4H3
H5H6
H2
H1
C1
H3
H2
H1
C1 C2
H4H3
H5H6
H2
H1
C1
H3
H2
A- Représentation de CRAM
C
HH
H
H
C C
H
H
H
HH
HDans
le plan
Vers l’avant
Vers
l’arrière
B- Projection de NEWMAN
H1
C1 C2
H4H3
H5H6
H2
On observe la molécule selon une liaison
(souvent C-C) choisie : on projette les
groupes substituants dans le plan
perpendiculaire à la liaison
H1
C1 C2
H4H3
H5H6
H2
H
H
H
H
H
H
C- Perspective Cavalière
Vers l’avant
Vers
l’arrière H1
C1 C2
H4H3
H5H6
H2C1
C2
H3H2
H1
H6 H5
H4
Vers l’avant
Vers
l’arrière
II- Modes de représentation spatiale des molécules
5
A- Description
Rappel: des isomères conformationnels sont des stéréoisomères obtenus par
simple rotation autours de liaisons simples.
On introduit alors l’angle dièdre j , angle entre 2 plans ou 4 atomes :
On va étudier l’énergie potentielle en fonction de j.
Le but : on recherche les formes les plus stables (minima d’énergie potentielle) :
les conformères, qui différent d’une conformation qui peut avoir n’importe
quelle énergie.
AC
C Bj
III- Conformations : analyse conformationnelle
6
H
H
HH
H
H
B- ETHANE
Epot
(kJ.mol-1)
CR=φ
0° 60° 120° 180° 240° 300° 360°
H
H
H
H
H
H
Conformations
éclipsées
conformères
Décalé
H
H
H
H
H
H
H
H
H
H
H
H
H
H
HH
H
H
H
H
HH
H
H
12.5
7
C- BUTANE
Epot
CR=φ
CH3
H
HH
CH3
H
0° 60° 120° 180° 240° 300° 360°
CH3
H
H
H
CH3
H
H
CH3
HH
CH3
H
H
CH3
H
H
CH3
H
H
H3C
HH
CH3
H
H3C
H
H
H
CH3
H
Conformations
éclipsées
2 conformères
Décalés gauches
1 conformère
Décalé anti
8
III-D- CYCLOHEXANE
C1C6
C5
C4 C3
C2
HaHe
Ha
He
Ha
Ha
He
He
Ha
He
Ha
HeC1
C6C5
C4 C3
C2
POSITION AXIALE
POSITION EQUATORIALE
PLAN MOYEN DU CYCLE
C1C6
C5
C4 C3
C2
Représentation des
liaisons équatoriales
AIDEZ VOUS des CARREAUX
de votre FEUILLE
1- le cyclohexane
9
Conformation
Bateau
2 Conformères
Chaise
CR
Epot
I II
Projection de Newman
selon C2-C3 et C6-C5
C4
H H
C1
C3
C5
C2
C6
10
1
2
3
4
5
6
1
2
3
4
5 6
L'équilibre d'interconversion des 2 chaises inverse les position des H.
Les axiaux deviennent équatoriaux et inversement.
Projection de Newman selon C2-C3 et C6-C5
11
2- le cyclohexane monosubstitué
Quel est le conformère le plus stable ?
C4
H
H
C6
H
C1Cl
H
H
C2
H
H C4
H
H
C6
Cl
C1H
H
H
C2
H
H
H
H
H
H
H
H
H
Cl
H
H
H
H
H
H
H H
H
H
H
H
H
H
H
Cl
1
1 2 3
4
5 6
2 3
4 5
6
12
Substituant - Br - CH3 -tBu
ΔE=Eax-Eeq
(kJ.mol-1) 1.7 7.2 21
La chaise avec tBu est bloquée à 100% en équatoriale car tBu est très volumineux.
Br
Br
Substituants en position trans
Substituants en position cis
Cas polysubstitué : les effets sont additifs !!!
Def : substituants en position trans : de part et d’autre du plan moyen du cycle.
substituants en position cis : du même du plan moyen du cycle.
2- le cyclohexane disubstitué
13
1- carbone asymétrique A- Exemples
Def : un carbone est dit asymétrique si il porte 4 substituants différents, il est noté C*.
C*
C*
Image dans un miroir
C*
Def :
2 stéréoisomères de
configuration image
l’un de l’autre dans un
miroir forment un
couple d’énantiomères
C*
HO H
COOH
CH3
IV- Configurations
14
C C
Cl
H
Cl
H
C C
Cl
H
H
Cl
Def : 2 stéréoisomères de configuration NON image l’un de
l’autre dans un miroir forment un couple de
diastéréoisomères
Rmq: Il n’y a aucun C* puisque les C ne portent que 3
susbstituants !!!
Comment les différencier formellement ? Règles CIP !
2- les doubles liaisons
15
B- REGLES DE PRIORITÉ DE CAHN, INGOLD, PRELOG
DES SUBSTITUANTS : REGLES CIP
Objectif : déterminer l’ordre de priorité des 4 substituants attachés à un carbone asymétrique :
Dans cette section, a est prioritaire sur b qui l’est sur c qui l’est sur d : a > b > c > d
Les substituants directement liés à l‘atome qu’on considère sont dits substituants de rang 1.
Les atomes liés aux atomes de rang 1 sont dits de rang 2 et ainsi de suite.
1) La priorité des atomes va dans le sens décroissant de leur numéro atomique Z.
Ex :
rq: pour des atomes isotopes, la priorité est donnée
par le A le plus grand, ex D>H
C
H
ClH3C
OH
C
C
H
Cl
O
16
2) En cas d’égalité au rang 1, on compare les substituants de rang 2 des atomes de même priorité.
On classe les substituants de rang 2 par priorité décroissante. On compare dans l‘ordre décroissant les substituants de même priorité de chaque atome. Dès que l‘indétermination est levée, on arrête.
Si l’indétermination n’est pas levée au rang 2, on continue en allant au rang 3.
3) Une liaison multiple équivaut à plusieurs liaisons simples entre deux atomes.
Ainsi : équivaut à Les atomes (C) et (O) sont des
atomes répliques.
Précisément dans une liaison multiple entre deux atomes A et B, on rattache à chaque
atome A et B autant de répliques B ou A de l’autre atome qu’il y a de liaisons entre A
et B. Ces répliques portent des atomes fantômes.
H3C C1
CH3
CH3
C2
Cl
C3
H
Cl
H
H
Ex :
H3C
C
O
H
(O)
(C)
H3C
O
H
17
exemples :
• identifier tous les C* et classer leurs substituants selon les règles CIP.
– 1)
– 2)
– 3)
OH OCH3
CH3
18
• Composés à 1 C* : énantiomérie
On regarde la molécule dans l’axe C*-d
– Si pour aller de a, vers b puis vers C, on tourne dans le Sens des aiguilles d’une montre le C* est dit Rectus noté R, sinon Sinister : S.
– On dit alors que les molécules R et S sont un couple d’énantiomères.
– Elles sont image l’une de l’autre dans un miroir.
– trouver la configuration absolue du C* de l’ex 2 précédent.
– Astuce : si le groupement d n’est pas à l’arrière, casser VIRTUELLEMENT la liaison C-d et l’inverser avec celle qui est à l’arrière. Déterminer la configuration absolue du C* obtenu. La vraie configuration absolue est l’inverse.
En effet pour passer d’un C* R à un C* S, il faut casser 2 liaisons et les inverser.
C- Nomenclature : configuration absolue d’1 C*
C
a
b c
d
C
a
b c d
19
• Composés à plusieurs C* : diastéréoisomérie
– On fait le même travail pour chaque C*
C C
HO H
H3C COOHOHH
C CHO H
H OHCOOHH3C CC
OHH
CH3HOOCHO H
C CH3C H
HO COOHOHH
C CH3C H
H OHCOOHHO
CCCH3H
OHHOOCHO H
Relation d’énantiomérie
Relation de diastéréoisomérie C C
OH H
H3C COOH
OHH
20
• Cas particulier : molécule symétrique
C C
HO OH
HOOC COOHHH C C
HO OH
H HCOOHHOOC CC
OHHO
COOHHOOCH H
C CHOOC OH
HO COOHHH C C
HOOC OH
H HCOOHHO CC
COOHHO
OHHOOCH H
Relation d’énantiomérie
Relation de diastéréoisomérie
C C
OH H
HOOC COOH
OHH
S R
21
En réalité
Il n’y a que 3 stéréoisomères
de configuration.
C C
HO OH
HOOC COOHHH C C
HO OH
H HCOOHHOOC= = Le composé
méso
C C
HO OH
HOOC COOHHH
C CHOOC OH
HO COOHHH C C
HOOC OH
H HCOOHHO
Relation d’énantiomérie
Relation de diastéréoisomérie
22
D- Composés à double liaison C=C, avec substituants
différents
– Classer les 2 substituants des 2 C selon les règles CIP
– si les 2 groupements prioritaires sont du même coté de la
double liaison, elle est dite Z (zusamen), sinon elle est dite
E (entgegen).
– Autre nomenclature : par analogie avec cyclohexane
disubstitué, on dit aussi qu’une double liaison C=C Z est
Cis et que la E est trans.
C C
ClH3C
CH3H
C C
Cl
H3C CH3
H
23
E- Nombre de stéréoisomères de configuration :
– soit n le nombre de C* de la molécule
– soit p le nombre de C=C ayant une isomérie Z/E
• Le nombre maximal de stéréoisomère de
configuration est : 2n+p – ex : donner le nombre maximal de stéréoisomères et
les identifier :
OH OCH3
24
F- Applications :
• Donner les relations entre A et les autres molécules (énantiomères,
diastéréoisomères, identiques )
C CHO H
H OHClH3C
A
C CHO H
H ClOHH3C
B
C CHO
HH3C
OHCl
H
C
C CH3C
HH
OHCl
HO
D
C CHO H
H OHClH3C
E
C CHO H
H ClOHH3C
F
25
A-Expérience - Loi de BIOT
α
Lumière blanche
NON polarisée polariseur
analyseur
Lumière polarisée
II0cosα
la loi de BIOT : = []D20.l.c
-[]D20 pouvoir rotatoire spécifique de l’espèce étudiée.
(D : raie D du sodium ; 20 : à 20°C)
- c : concentration en l’espèce optiquement active. - l: longueur de la cuve (usuellement en dm, pour []D
20
en (°.dm-1.(g.mL-1)-1) et c en (g.mL-1))
l
Pour un observateur qui
reçoit la lumière : si le plan
est dévié :
-vers la droite la solution
est dextrogyre (d) ou (+)
- vers la gauche lévogyre
(l) ou (-).
V- Isomérie optique : propriétés des isomères de configuration
26
Cl Cl
OH
H
OH
H
• Toute molécule optiquement active est chirale. Un objet est dit chiral si il
est différent de son symétrique dans un miroir
• Identifier les objets chiraux :
B- Molécule optiquement active
Rmq: tout objet qui possède un plan ou un centre de symétrie est achiral (NON chiral)
car identique à son image dans un miroir 27
1- Enantiomérie • Couple d’énantiomère : 2 isomères de configuration image l’un de l’autre dans un miroir.
• Ex : (R)-butan-2-ol et (S)-butan-2-ol
• Propriétés physiques :
• NON SEPARABLES !!!
• Les énantiomères ont des pouvoirs rotatoires spécifiques opposés : si l’un est dextrogyre
l’autre est lévogyre.
• AUCUN LIEN ENTRE (R, S) et (+, -) :
Ex : (S) butan-2-ol est + cad dextrogyre
(S) glyceraldéhyde est – cad levogyre
C- Enantiomérie - diastéréoisomérie
Tfus (°C) Densité pKa [a]D
(°.dm-1.(g.mL-1)-1)
(R) Butan-2-ol -87 0.80 17 - 13.52
(S) Butan-2-ol - 87 0.80 17 + 13.52
On le précise dans le nom :
(S)-(-)-glyceraldéhyde 28
• Définition : un mélange équimolaire d’énantiomères s’appelle un mélange racémique
– Conséquence : racémique=
le mélange racémique est optiquement inactif
• rmq : si on trouve un pouvoir rotatoire nulle
– molécule optiquement inactive
– ou mélange racémique
• Excès énantiomérique :
– Pour un mélange des deux énantiomères en proportions quelconque, on
définit l’excès énantiomérique (noté e.e.) (en notant [R] et [S] les
concentrations des formes R et S dans la solution) par :
(on exprime souvent ce résultat en pourcentage)
– Valeur de e.e. : 0 ≤ e.e. ≤ 1
– e.e. = 1
– e.e. =0
][][
][][..
SR
SRee
29
Tfus (°C) 287 135 172 172 147
pKa 3.0 & 4.4 1.9 & 6.1 3.0 & 4.3 3.0 & 4.3 3.2 & 4.8
[a]D
(°.dm-1.(g.mL-1)-
1)
0 0 + 12.7 - 12.7 +17.8
HOOC COOHHOOC
COOH
• Diastéréoisomères = isomères de configuration, NON images dans un miroir.
• Ex : alcènes, molécules avec plusieurs C*
• Deux diastéréoisomères ont des propriétés physiques différentes :
températures de changement d’état différentes, densité différentes,
solubilités différentes dans différents solvants, … ils sont séparables
• Les valeurs absolues de leurs pouvoirs rotatoires spécifiques sont aussi
différentes.
• Rmq : le pouvoir rotatoire spécifique du composé méso est nul, car il est
achiral.
2- Diastéréoisomères
C CHOOC OH
HO COOHHH
R R
C CHOOC OH
H HCOOHHO
S S
C C
HO OH
HOOC COOHHH
S R
30
3- Séparation d’énantiomères
• Résolution d’un racémique : séparation des 2 énantiomères d’un mélange
racémique par l’obtention temporaire d’un mélange de diastéréoisomères,
donc séparables physiquement.
XR + XS
(mélange
racémique)
YS
(optiquement pur)
XRYS + XSYS
XRYS
XSYS
XR + YS
XS + YS
XR
XS
31
• (S) limonène : odeur de citron ≠ (R) limonène : odeur d’orange
• Thalidomide : (R) anti-nauséeux ≠ (S) tératogène
• ibuprofène : Seul l'énantiomère S possède une activité médicamenteuse
efficace (le R est trois fois moins puissant).
• vitamine C : seul le lévogyre a une efficacité
• acide α-aminé : quasi toujours S
D- chiralité et monde du vivant
CH
H2N COOH
R 32




































![7 - Cours isomérie 09 [Mode de compatibilité] · Stéréoisomérie n’est perceptible que sur une vue tridimensionnelle – Deux types • Enantiomérie • Diastéréoisomérie.](https://static.fdocuments.fr/doc/165x107/5b9c173109d3f2194e8bab99/7-cours-isomerie-09-mode-de-compatibilite-stereoisomerie-nest-perceptible.jpg)




![7 - Cours isomérie 09 [Mode de compatibilité]chimiephysique.net/images/site/ChimieUniversitaire/organique/7.pdf · 2. Composés cycliques : isomérie cis/trans • Cas des substituants](https://static.fdocuments.fr/doc/165x107/5e1bbd486797ed49df23642c/7-cours-isomrie-09-mode-de-compatibilit-2-composs-cycliques-isomrie.jpg)